题目内容
【题目】镓是一种放在手心就会熔化的金属。如①是镓元素在元素周期表中的部分信息,②是镓原子的结构示意图。请回答:
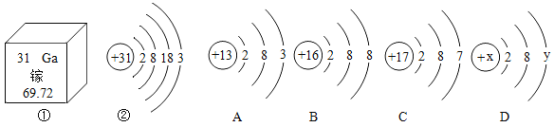
(1)镓原子的相对原子质量为______________,镓原子位于元素周期表中第________周期。
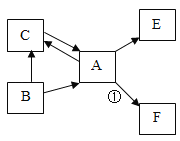
(2)A、B、C三种微粒所属元素中与镓元素化学性质相似的是________(填“A”、“B”或“C”),则镓离子与B粒子形成的化合物的化学式为________________。
(3)D为某粒子的结构示意图若x-y=12时,该粒子的符号为______________(用化学用语表示)。
【答案】69.72 四 A Ga2S3 Ca2+
【解析】
(1)元素周期表中的一格可知:汉字下面的数字表示相对原子质量。镓原子的相对原子质量为69.72,根据镓原子结构示意图可知,镓原子核外有4个电子层,元素周期表中,电子层数与周期数在数值上相等,镓原子位于元素周期表中第四周期;
(2)元素的化学性质与最外层电子数的关系密切,A、B、C三种微粒所属元素中与镓元素化学性质相似的是A,它们的最外层电子数相等;镓原子最外层电子数为3,在化学反应中易失去3个电子,形成带3个单位正电荷的离子,B粒子是带2个单位负电荷的硫离子,镓离子与B粒子形成的化合物的化学式为Ga2S3;
(3)当该粒子是原子时x-y=10,故该粒子不是原子是离子,是离子y=8,所以x=20,因此D是钙离子,符号为Ca2+。

【题目】某一天,下列城市的空气质量监测数据如下表
城市 | 污染指数 | 首要污染物 |
北京 | 81 | 二氧化硫 |
上海 | 117 | 可吸入颗粒 |
广州 | 186 | 二氧化氮 |
东莞 | 173 | 可吸入颗粒 |
重庆 | 201 | 二氧化硫 |
昆明 | 48 | 可吸入颗粒 |
空气质量分级标准如下表
污染指数 | 0~50 | 51~100 | 101~200 | 201~300 | >300 |
质量级别 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
质量状况 | 优 | 良 | 轻度污染 | 中度污染 | 重度污染 |
请回答
(1)当天,以上城市中,污染最严重的是_____,东莞的空气质量级别是_____;
(2)北京的首要污染物是_____,它溶于雨水,会与水反应,生成亚硫酸(H2SO3);形成酸雨,请写出该反应的文字表达式:_____
(3)请说出一条防治空气污染的措施:_____ 。