题目内容
【题目】有一瓶未知浓度的氢氧化钠溶液,同学们想用10%的稀盐酸来测定其溶质的质量分数。以下是两组同学的设想及做法:
①甲组同学的实验如下图所示:在烧杯中加入5g氢氧化钠溶液,滴入2滴酚酞溶液,用滴管慢慢滴入10%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止。
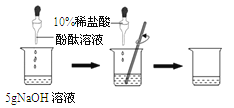
请回答:
酚酞溶液的作用是 ⑿ 边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是 ⒀ 。
当溶液颜色恰好变为无色时,共用去了稀盐酸14.6g,则甲组这瓶氢氧化钠溶液中溶质的质量分数为
⒁ (写出计算过程,结果用百分数表示)。
②乙组同学的设想是:在烧杯中加入一定量的氢氧化钠溶液,用滴管慢慢滴入10%的稀盐酸,并不断搅拌,通过用pH试纸多次测定溶液pH的办法,达到实验目的。
下列使用pH试纸的方法正确的是 ⒂ (填字母)。
A.将pH试纸剪成几段节约使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸润湿后放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上
在滴加稀盐酸一段时间后,发现溶液中有少量气泡产生。他们通过进一步实验证明:该组用的这瓶氢氧化钠溶液已经部分变质。请你根据他们的实验步骤写出实验现象:
实验步骤 | 现 象 | 结 论 |
取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液。 | ⒃ | NaOH溶液部分变质 |
若要除去溶液中变质生成的杂质,请简要写出实验方案 ⒄ 。
【答案】⑿ 判断反应是否恰好完成(或证明两者发生了反应等)
⒀ 使反应物充分接触,完全反应
⒁ 32%
⒂ A C
⒃ 产生白色沉淀,酚酞变红
⒄ 加入适量Ba(OH)2溶液【或Ca(OH)2溶液】恰好反应(或刚好不再产生沉淀),过滤。
【解析】
试题分析:①酚酞溶液为酸碱指示剂,所以判断反应是否恰好完成(或证明两者发生了反应等);边要用玻璃棒不断搅拌的目的是使反应物充分接触,完全反应;当溶液颜色恰好变为无色时,共用去了稀盐酸14.6g,则甲组这瓶氢氧化钠溶液中溶质的质量分数
解:HCl物质的量:14.6g×10%÷36.5=0.04mol……(1分)
设氢氧化钠为x mol
NaOH + HCl → NaCl + H2O (1分)
1 1
x 0.04mol
1:1=x:0.04mol
x=0.04mol (比例式和答案共1分)
0.04×40÷5×100%=32% (1分)
答:略
②乙组:下列使用pH试纸的方法正确的是A.将pH试纸剪成几段节约使用;C.将pH试纸放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上;该组用的这瓶氢氧化钠溶液已经部分变质。产生白色沉淀,酚酞变红证明已部分变质;若要除去溶液中变质生成的杂质,必须出去碳酸根离子,但不能引进新杂质,故加入适量Ba(OH)2溶液【或Ca(OH)2溶液】恰好反应(或刚好不再产生沉淀),过滤。即可。

【题目】铀235是核电站的主要燃料,其原子序数为92,相对原子质量为235。下列有关说法正确的是
A.铀属于非金属元素 B.该原子的核电荷数为92
C.该原子核内有92个中子 D.该原子核外有143个电子
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有KOH溶液的小烧杯中.
【学生板演】该反应的化学方程式 (23) .
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有K2SO4
猜想二:有K2SO4和H2SO4
猜想三:有K2SO4和KOH
猜想四:有K2SO4、H2SO4和KOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 (24) .
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 (25) .
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
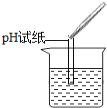
实验操作 |
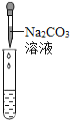
|
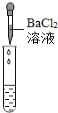
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【得出结论】通过探究,全班同学一致确定______(26)__________是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出
【实验探究】(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是 (27) .
(2)实验方案中也有一个是错误的,错误的原因是 (28)