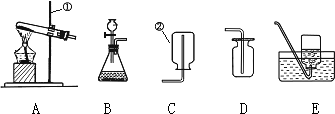
题目内容
(1)为测定某地方的空气中SO2和可吸入颗粒的含量,查阅资料得知:可用含有一定量碘的溶液测定空气中的SO2含量,反应方程式是:SO2+I2+2H2O=H2SO4+2HI.甲同学设计了如下图所示的实验装置:

①应用上述装置测定空气中的SO2含量和可吸入颗粒的含量,除测定气体流速(单位:cm3/min)外,还需要测定吸收前后颗粒吸附剂、棉花、盛放容器的总质量和 .
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度.请你协助甲同学完成稀碘溶液的配制:
第一步:准确称取1.27g碘单质加入烧杯中, ;
第二步:加适量水使之完全溶解,然后加水至溶液体积为1000mL;
第三步:从第二步所得溶液中,取出10.00mL溶液加入稀释至100mL.
(2)乙同学拟用下列简易装置测定空气中的SO2含量:准确取50mL第三步所得的碘溶液,注入右图所示广口瓶中,加2~3滴淀粉指示剂,此时溶液呈蓝色.在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n).
假设乙同学的测量是准确的,乙同学抽气的次数为80次,计算说明该地空气中的SO2含量是否符合排放标准.

(3)该小组同学认为这些工厂要对排出的废气进行处理,为了达到最好效果,在实验室进行了实验模拟,你认为他们为了吸收产生的SO2气体,所使用药品应该是 ,发生的化学反应方程式
经过再三思考,设计了以下装置,认为下列哪种不能采用 ,因为其他装置都具有 作用.
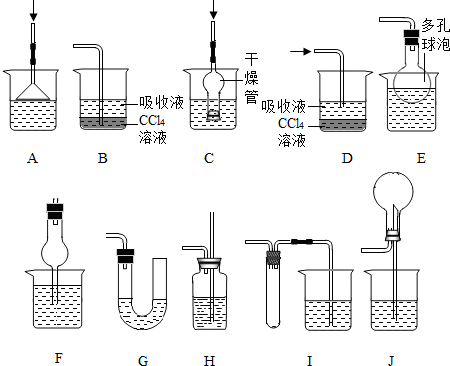

①应用上述装置测定空气中的SO2含量和可吸入颗粒的含量,除测定气体流速(单位:cm3/min)外,还需要测定吸收前后颗粒吸附剂、棉花、盛放容器的总质量和
②已知:碘单质微溶于水,KI可以增大碘在水中的溶解度.请你协助甲同学完成稀碘溶液的配制:
第一步:准确称取1.27g碘单质加入烧杯中,
第二步:加适量水使之完全溶解,然后加水至溶液体积为1000mL;
第三步:从第二步所得溶液中,取出10.00mL溶液加入稀释至100mL.
(2)乙同学拟用下列简易装置测定空气中的SO2含量:准确取50mL第三步所得的碘溶液,注入右图所示广口瓶中,加2~3滴淀粉指示剂,此时溶液呈蓝色.在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n).
假设乙同学的测量是准确的,乙同学抽气的次数为80次,计算说明该地空气中的SO2含量是否符合排放标准.

(3)该小组同学认为这些工厂要对排出的废气进行处理,为了达到最好效果,在实验室进行了实验模拟,你认为他们为了吸收产生的SO2气体,所使用药品应该是
经过再三思考,设计了以下装置,认为下列哪种不能采用

考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:科学探究
分析:(1)测定SO2含量,除测定气体流速(单位:cm3?min-1)外,还需要测定开始到碘溶液刚好变成无色的时间,要测可吸入颗粒的含量,可用颗粒吸附剂来吸收,颗粒吸附剂前后质量之差即为可吸入颗粒的质量,则应测定吸收前后颗粒吸附剂、棉花、盛放容器的总质量;准确称取1.27g碘单质加入烧杯中,同时还应加入少量碘化钾固体,根据碘的质量和浓度判断所需容量瓶的容积;
(2)二氧化硫用碘溶液来吸收,方程式为:SO2+I2+2H2O═2HI+H2SO4,结合反应的方程式计算,为减少实验误差,应减少碘溶液浓度或缩小容器体积.
(3)根据二氧化硫是酸性氧化物,和氢氧化钠反应生成亚硫酸钠和水解答;根据二氧化硫溶于水,也会使水面上升,发生倒吸解答.
(2)二氧化硫用碘溶液来吸收,方程式为:SO2+I2+2H2O═2HI+H2SO4,结合反应的方程式计算,为减少实验误差,应减少碘溶液浓度或缩小容器体积.
(3)根据二氧化硫是酸性氧化物,和氢氧化钠反应生成亚硫酸钠和水解答;根据二氧化硫溶于水,也会使水面上升,发生倒吸解答.
解答:解:
(1)①要测可吸入颗粒的含量,可用颗粒吸附剂来吸收,颗粒吸附剂前后质量之差即为可吸入颗粒的质量,则应测定吸收前后颗粒吸附剂、棉花、盛放容器的总质量,测定SO2含量,除测定气体流速(单位:cm3?min-1)外,还需要测定开始到碘溶液刚好变成无色的时间,二氧化硫用碘溶液来吸收,方程式为:SO2+I2+2H2O═2HI+H2SO4;
②由题意可知碘单质微溶于水,KI可以增大碘在水中的溶解度,则准确称取1.27g碘单质加入烧杯中,同时还应加入少量碘化钾固体,加适量水搅拌使之完全溶解,n(I2)=
=0.005mol,
而配制100mL 5×10-4mol?L-1碘溶液,
则第二步操作应将第一步所得溶液全部转入1000 mL的容量瓶中,定容,摇匀,浓度为5×10-3mol?L-1,
则从第二步所得溶液中,取出10.00mL溶液于100mL容量瓶中,加水稀释至刻度线,可得浓度为5×10-4mol?L-1碘溶液,
故答案为:再加入适量KI;
(2)设反应的SO2质量为x
SO2+I2+2H2O=H2SO4+2HI
64 254
x 1.27×10-2×0.5g
=
解得:x=1.6×10-3g=1.6 mg
(1.6mg)/(80×100×10-3L)=0.2 mg/L 不符合排放标准
(3)二氧化硫是酸性氧化物,和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH═Na2SO3+H2O;
二氧化硫溶于水,也会使水面上升,易发生倒吸,故选D
答案:
(1)①测定开始到碘溶液刚好变成无色的时间②再加入适量KI
(2)不符合排放标准
(3)NaOH溶液 SO2+2NaOH═Na2SO3+H2O D 防倒吸
(1)①要测可吸入颗粒的含量,可用颗粒吸附剂来吸收,颗粒吸附剂前后质量之差即为可吸入颗粒的质量,则应测定吸收前后颗粒吸附剂、棉花、盛放容器的总质量,测定SO2含量,除测定气体流速(单位:cm3?min-1)外,还需要测定开始到碘溶液刚好变成无色的时间,二氧化硫用碘溶液来吸收,方程式为:SO2+I2+2H2O═2HI+H2SO4;
②由题意可知碘单质微溶于水,KI可以增大碘在水中的溶解度,则准确称取1.27g碘单质加入烧杯中,同时还应加入少量碘化钾固体,加适量水搅拌使之完全溶解,n(I2)=
| 1.27g |
| 254g/mol |
而配制100mL 5×10-4mol?L-1碘溶液,
则第二步操作应将第一步所得溶液全部转入1000 mL的容量瓶中,定容,摇匀,浓度为5×10-3mol?L-1,
则从第二步所得溶液中,取出10.00mL溶液于100mL容量瓶中,加水稀释至刻度线,可得浓度为5×10-4mol?L-1碘溶液,
故答案为:再加入适量KI;
(2)设反应的SO2质量为x
SO2+I2+2H2O=H2SO4+2HI
64 254
x 1.27×10-2×0.5g
| 64 |
| 254 |
| x |
| 1.27g×10-2×0.5g |
解得:x=1.6×10-3g=1.6 mg
(1.6mg)/(80×100×10-3L)=0.2 mg/L 不符合排放标准
(3)二氧化硫是酸性氧化物,和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH═Na2SO3+H2O;
二氧化硫溶于水,也会使水面上升,易发生倒吸,故选D
答案:
(1)①测定开始到碘溶液刚好变成无色的时间②再加入适量KI
(2)不符合排放标准
(3)NaOH溶液 SO2+2NaOH═Na2SO3+H2O D 防倒吸
点评:本题考查物质含量测定的实验设计,侧重于学生的分析能力、计算能力和实验能力的考查,为高考常见题型,注意把握实验原理,结合方程式计算该题,难度中等.

练习册系列答案
相关题目