题目内容
【题目】同学们利用“硫酸、硝酸铵、氢氧化钠、碳酸钾”四种物质的溶液进行探究学习,完成下列各问:
(实验探究)
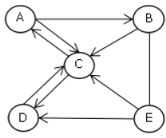
(1)A、B、C、D四组同学分别进行了下列实验
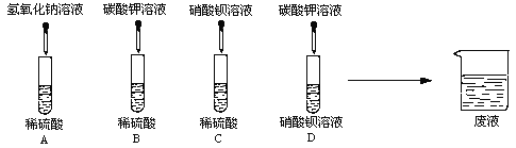
写出下列的两个化学方程式:
①A中的反应______________________
②D中的反应_____________________________
(挖掘实质)
下图是A组反应的微观过程示意图该化学反应的实质可以表示为H++OH-=H2O
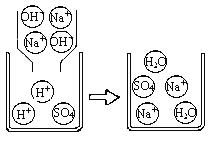
(实践运用)
完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
(1)①溶液中的白色沉淀一定是______________________,理由:___________________________
(2)废液中一定含有的离子是____________________,一定不含有的离子是_______________________
(3)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证
溶液中可能含有的离子 | 实验步骤 | 实验现象 | 实验结论 |
可能含有_________ | ②取滤液滴______________ | 现象明显 | 含有该离子 |
【答案】2NaOH+H2SO4=Na2SO4+2H2O K2CO3+Ba(NO3)2=BaCO3↓+2KNO3 硫酸钡 无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,亦说明白色沉淀不能溶于酸 H+、Na+、K+和NO3- 氢氧根离子和碳酸根离子 Ba2+ 入少量硫酸钠溶液
【解析】
[实验探究]①A中的反应氢氧化钠和硫酸反应生成硫酸钠和水,方程式为2NaOH+H2SO4=Na2SO4+2H2O;
②D中的反应碳酸钾与硝酸钡反应生成碳酸钡和硝酸钾,方程式为:K2CO3+Ba(NO3)2=BaCO3↓+2KNO3;
[实践运用](1)无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,亦说明白色沉淀不能溶于酸,由“硫酸、硝酸铵、氢氧化钠、碳酸钾”四种物质看,沉淀一定是硫酸钡;
(2)由于无色溶液滴加紫色石蕊试剂,变为红色,说明得到无色溶液为酸性,酸过量,则溶液中一定不能含有氢氧根离子和碳酸根离子;通过上述探究发现,在溶液中H+和OH-不能大量共存,我还发现在溶液中Ba2+和SO42-也不能大量共存;利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液;经测定,该溶液显酸性;则在该溶液中一定含有的离子是H+、Na+、K+和NO3- ;
(3)根据分析可知方案如下,可能含有Ba2+,取上述溶液少量于试管中,加入少量硫酸钠溶液,若出现白色沉淀,则说明上述溶液中含有Ba2+;若没有出现白色沉淀,则说明上述溶液中不含有Ba2+;可能含有SO42-,取上述溶液少量于试管中,加入少量硝酸钡溶液,若出现白色沉淀,则说明上述溶液中含有SO42-;若没有出现白色沉淀,则说明上述溶液中不含有SO42-。

 阅读快车系列答案
阅读快车系列答案