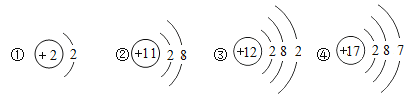��Ŀ����
����Ŀ��Ϊ�˴ﵽ�վ����Ͻ��ܼ��ŵ�Ŀ�ģ��Ӻ��н���þ������ͭ�ķ�ĩ�У��������ȡ����Ҫ����ԭ��MgSO4�����йؽ�����ʵ��������£�

��ش�
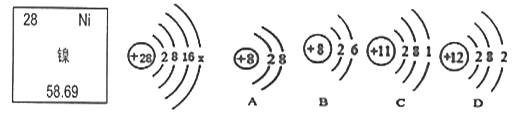
��1���������б����������Ľ���A��________����д��ѧʽ����
��2������a��������__________����������������Ҫʹ�ò��������������ǣ�___________��
��3��д����������漰�Ļ�ѧ��Ӧ����ʽ��__________________��
��4��ʵ�鲽����г��˼���ϡ�����⣬����ѡ�������Լ�________�����ţ���
a.����ͭ��Һ b.�Ȼ�����Һ c.��������Һ
��5���������ʵ�����̣�С��ͬѧ��Ϊͨ��ʵ��õ������ֽ����Ļ��˳��ΪMg>Fe>Cu������Ϊ�����ж϶������жϲ�˵���������_____________________
���𰸡�Fe ���� �����ֹ�ֲ��¶ȹ������Һ�ηɽ� Mg+H2SO4=MgSO4+H2�� a ���ԣ�þ�����Ľ������ǿ����û����֤
��������
��1��þ������ͭ�н��������Ա��������������Ľ�����������ѧʽΪ��Fe��
��2������a �ǽ������Һ�����IJ��裬���ǹ��ˡ��������Ĺ����У�Ϊ�˷�ֹҺ���⽦����Ҫ�ò��������ϵؽ��衣
��3��þ��ϡ���ᷴӦ��������þ����������Ӧ�ķ���ʽΪ��Mg+H2SO4=MgSO4+H2����
��4��þ��ͭ�������Ȼ��Ʒ�Ӧ���ʲ��������Ȼ�����Һ��þ��ͭ�����Ժ���������Ӧ��������þ�л�������þ������ͭ����ֻ��ѡa��
��5����ʵ����ֻ��֤��þ����ͭ�����ܵó�þ�����Ļ��ǿ�����ʲ���ȷ��

����Ŀ������ȼ�ŵ�С�������һ������ƿ�в���������ʱ������һ�����Ϩ���ˡ���ô������Ϊʲô��Ϩ���أ�ij��ѧ��ȤС�����������̽�������������ؿո�
��������롿���������ȼ�հѼ���ƿ�ڵ������ľ�����������Ϩ��
���������ȼ���漯��ƿ�������������Ͷ��������ų����������٣�ʹ�¶Ƚ��������____________________���£���������Ϩ��
���������ȼ�ղ����Ķ�����̼����𣬵�������Ϩ��
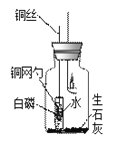
������ʵ�顿С���������ͼ��ʾ��ʵ��װ�ã�������ʵ������֤���롣
| ʵ����� | ʵ������ |
��ȼ������ͬ�����ϵ���������ҩƷһ����뼯��ƿ�У��������� | ���������������____ | |
����Ϩ������ȴ��ͭ˿���ᣬʹʢ����ͭ�������Թܿڣ��Թܵ��£�ˮ������ | һ��������Ż�ȼ�գ��д���____���� |
�����������ۡ�
��1������Ϩ��ǰ��Ҫ�ð���û��С�Թ���ʢ��ˮ�У�Ŀ����_________��
��2������ƿ��װ��һЩ��ʯ�ҵ����Ŀ�ģ�������������Ӧ���ƿ�ڵ�_____���÷�Ӧ�Ļ�ѧ����ʽΪ__________��
��3��ƿ�ڵİ�����ȼ�գ�֤������____��____���ܳ��������Ǹ��ݳ����IJ�����Ϊ��Ӧ�ðѡ�ȼ����Ҫ��������һȼ�շ�����������������Ϊ��____________����
����Ŀ��NH4C1��Na2SO4���ܽ�ȱ����ܽ���������¡�����˵���������
�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ�� S/g | NH4C1 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
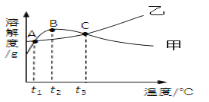
A. t2Ӧ����30�� ��50��
B. 10�� ʱ�����͵�Na2SO4��Һ��������������Ϊ9.6%
C. �ס��ұ�����Һ��t3���µ�t2�����ʵ�������������С
D. B�㡢C���Ӧ�ļ���Һ����������������С��ϵΪB��C
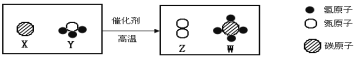
����Ŀ�����������ʼ�Ѱ�ҹ��ɣ���ѧ�û�ѧ�ķ���֮һ�����б����е��������ʣ�С��ͬѧ���������˹��ɣ�������������Ӧ���ݡ���˵������XΪ�������ʣ��ڹ��ɲ����ظ���
���� | �仯���� | X�Ļ�ѧʽ | ���й��� |
��1��Na��Al��Cu��Fe��X | ������ԣ���ǿ���� | _________ | Na��X��Al��Fe��Cu. |
��2��FeS��FeO��Fe3O4��X | ��������Ԫ�ص������������ɶൽ�� | Fe2O3 | ________________ |
��3��NH3��NO��NO2��N2��X | _______________ | N2O3 | NO2��N2O3��NO��N2��NH3 |