��Ŀ����
����Ŀ����19�֣����������������������е�Ӧ�÷dz��㷺��
��1���Ի���õĹ�������ͭ�Ͻ�����ģ���Ҫ����Ϊͭ�Ͻ���кܺõ� ������ţ���
A�������� B�������� C����չ��
��2��������ʴ����˷ѡ�����Ʒ��ʴ�Ĺ��̣�ʵ��������������е� �� ������ѧ��Ӧ�Ĺ��̡�
��3��Ŀǰ����������50%���ϵķϸ����õ��������ã���Ŀ���� ��
A����Լ������Դ B���������ɿ��� C����ֹ��������
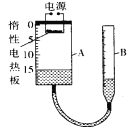
��4��������һ����Ҫ�IJ��ϣ������������������벻���������±���ʾ�˽������˳�����ͭ������������Ԫ�ر�������ģ���������õĴ������ޡ�
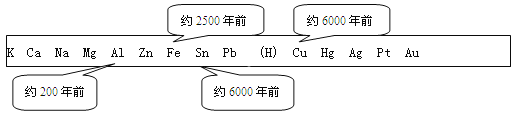
����ͼ�����ݺ��йصĻ�ѧ֪ʶ������Ϊ�������ģ���������õ��Ⱥ�˳������� �йء�
���ؿ��н���Ԫ�صĺ�����
�ڽ����ĵ����ԣ�
�۽����Ļ�ԣ�
�ܽ�������չ�ԣ�
�ݽ���ұ�������׳̶ȡ�
��5��ʵ������пƬ����Ƭ��ͭƬ��ϡ���ᡢ����п��Һ������������Һ������ͭ��Һ7�����ʣ�С��ѡ����ʵ����ʣ�������������ַ�����п��ͭ�����Ľ������˳�������֤��
�ٷ���һ��ѡ�õ�3�������� ������п��Һ������ͭ��Һ��
�ڷ�������ѡ�õ�3��������пƬ��ͭƬ�� ��
�۷�������ѡ��4��������пƬ����Ƭ��ͭƬ�� ��
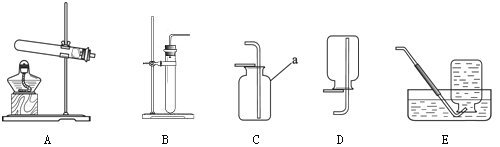
��6��������ԭ��������һ����̼����������Ӧ���䷴Ӧ�Ļ�ѧ����ʽΪ ����ʵ�����������ͼ��ʾװ�ý���ʵ�飺ʵ���в������ڵķ�ĩ�ɺ�ɫɫ���ɫ����ɫ��ĩ�������е���Ԫ�صĻ��ϼ�Ϊ ��
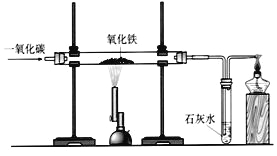
��7��ij������ÿ��������5 000 t��Fe2O3 80%�ij�����ʯ���ó������Ͽ��ղ���Fe 98%������ t��������������1λС����
��8��ij��ȤС���ͬѧ��һ��������Ʒ���������ʣ����ʲ�����ˮ��Ҳ����ϡ���ᷴӦ�����з������ס��ҡ�����λͬѧ�ֱ����ʵ�飬����һλͬѧ���õ�ϡ����������Ʒǡ����ȫ��Ӧ��ʵ�����������
�� | �� | �� | |
�ձ�+ϡ��������� | 200 | 150 | 150 |
����������Ʒ������ | 9 | 9 | 14 |
��ַ�Ӧ���ձ�+ʣ��������� | 208��7 | 158��7 | 163��7 |
��������������ݣ��ش��������⣺
�� ͬѧ���õ�ϡ������������Ʒǡ����ȫ��Ӧ��
������������Ʒ����������������(д����ϸ�ļ�����̣�
���𰸡���1��B ��2��ˮ������ ��3��A ��4���ۢݣ�
��5������Ƭ ������������Һ ��ϡ����
��6��3CO+Fe2O3![]() 2Fe+3CO2 ��+3��
2Fe+3CO2 ��+3��
��7��2857��1t
��8���� 93.3%
��������
�����������1���Ի���õĹ�������ͭ�Ͻ�����ģ���Ҫ����Ϊͭ�Ͻ���кܺõ����ԣ�
��2�����������������ˮ������ͬʱ�Ӵ���
��3���ϸ����������õ�Ŀ���ǽ�Լ������Դ��
��4���ɽ�����������ģ���������õĴ�������֪�������Ļ��Խ����Խ����ұ���Ľ��������õ�ʱ��Խ�磻
��5���ж�п��ͭ�����Ľ������˳����п������ͭ���жϽ�����Եķ����У�ȥ�м�Ľ��������߽�������Һ�����ߵĽ������м�Ľ����������ֽ����ֱ����ᷴӦ���ݽ������ᷴӦ�ľ��ҳ̶����жϽ����Ļ�ԣ�
��6��ʵ����������ԭ����һ����̼��ԭ�����������ɵ������Ͷ�����̼��3CO+Fe2O3 =====2Fe+3CO2 ������������Ԫ��Ϊ-2�ۣ����ݡ��ڻ������У��������ϼ۵Ĵ�����Ϊ�㡱��ԭ��֪����������Ԫ�صĻ��ϼ�Ϊ+3�ۣ�
��7�����û�ѧ����ʽ�����������������ɼ�������ɵ�����������
�����ɵ���������Ϊx��
5 000 t��Fe2O3 80%��������������=5000t��80%=4000t
3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
160 112
4000t x
160��112 =4000t��x
X=2800t
��Fe 98%������������=2800t��98% =2857.1t
��8�����ɱ�����Ϣ��֪���Һͱ��мӵ�ϡ�����������һ���ģ������Ҽ��������Ʒ����������7g����Ӧ�����ʵ�������Ҳ����7g��˵�������7g��Ʒ�е���û�з�����ѧ��Ӧ������������������ǡ����ȫ��Ӧ�ģ�
���������ᷴӦ���ɵ����������������������ٵ������������ɵ����������������û�ѧ����ʽ���ɽ�����������Ӧ�������ȼ��ɼ������Ʒ������������
���ɵ�����������=150g+9g-158.7g=0.3g
����Ʒ����������Ϊx,
Fe + H2SO4 == FeSO4 + H2��
56 2
X 0.3g
56��2 =x��0.3g
X=8.4g
��Ʒ��������������=8.4g��9g ��100% =93.3%
����