题目内容
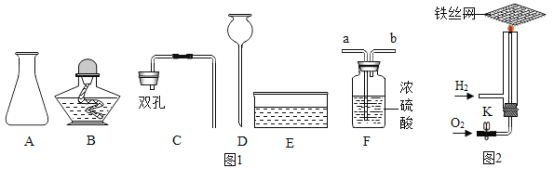
【题目】如图所示是某化学小组部分实验过程的装置图:
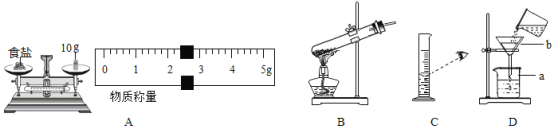
(1)写出标号仪器的名称:a________,b_______。
(2)A图中所称食盐的质量为_______g,若食盐与砝码的位置颠倒了,游码显示仍为A图,则食盐的实际质量为_______g。
(3)如图B所示操作,可能造成的后果是_______。
(4)欲量取40mL水,应选用的仪器是50mL的量筒和_______,某同学如C图读数,则实际量取的液体_______40mL(填“大于”“小于”或“等于”)。
(5)指出D操作可能造成的后果_______。
(6)如图所示,实验室要加热约150mL的水,要完成该实验需要准备的仪器有___(填序号)。
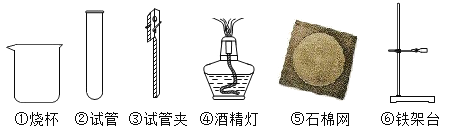
【答案】烧杯 漏斗 12.4 7.6 试管炸裂 胶头滴管 小于 液体溅出 ①④⑤⑥
【解析】
(1)据图可知仪器a是烧杯;b 是漏斗;
(2)A图中所称食盐的质量为10g+2.4g=12.4g;
由左盘的质量=右盘的质量+游码的质量可知:砝码质量=药品质量+游码的质量,所以药品质量=砝码质量-游码质量,即:药品的质量=10g-2.4g=7.6g;
(3)给试管中的固体加热时,为了防止冷凝水倒流、造成试管炸裂,试管口要略向下倾斜;图示操作可能导致试管炸裂;
(4)欲量取40mL水,应选用的仪器是50mL的量筒和胶头滴管,某同学如C图俯视读数,则实际量取的液体小于40mL;
(5)在过滤操作中,没有用玻璃棒引流可能会造成液体洒落;漏斗的下端没有紧靠烧杯内壁,可能会导致液体溅出;
(6)要有盛水的容器,应在烧杯和试管中选取,但是用水量为150mL,由给试管中的液体加热时,试管中的液体不能超过试管容积的三分之一,则要选择450mL以上的试管,这不可能,所以用烧杯;用烧杯给水加热选择支持固定仪器,要用铁架台;由于烧杯底面积大,易受热不均而炸裂,所以还要用石棉网;量取水的体积用量筒;酒精灯是热源仪器,加热必须选择酒精灯。所以要选择①④⑤⑥。

【题目】下面是兴趣小组同学对暴露在空气的氢氧化钠固体的探究。请回答下列问题:
(提出问题)
该氢氧化钠固体有没有变质?
(进行实验)
甲同学取少量固体于试管中用足量的水溶解,后加入少量的氯化钙溶液,观察到__________,证明氢氧化钠固体已经含有碳酸钠。
(提出问题)
如何除去氢氧化钠固体中的杂质,得到纯净的氢氧化钠呢?
(进行实验)
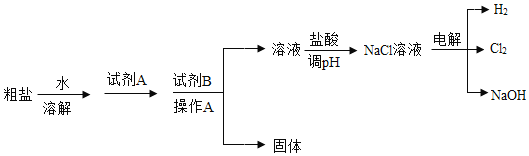
乙同学对该氢氧化钠固体进行提纯,按如下操作流程进行实验:

(实验分析)
(1)步骤②的主要操作名称是__________,步骤②中的反应的化学方程式是__________。
(2)步骤②中加入稍过量的氢氧化钙目的是__________。
(3)为获得纯净的氢氧化钠,步骤③所包含的具体操作是蒸发浓缩、__________(选填“蒸发结晶”或“降温结晶”)、过滤。
(4)丙同学认为乙同学流程中的氢氧化钙微溶于水,需要使用较大量的水,提高蒸发难度,可以用_______试剂代替。
(实验拓展)
如何测定久置的烧碱样品中氢氧化钠的质量分数?
从一瓶久置的烧碱中称取20g,干燥后剩余固体固体质量为19g,完全溶于水中配成100g样品溶液,现取一定溶质的质量分数的氯化钡溶液与样品溶液混合,充分反应后得到如表所示的数据。
项目和次数 | 第1次 | 第2次 | 第3次 | 第4次 |
样品溶液质量(g) | 10 | 20 | 30 | 40 |
氯化钡溶液质量(g) | 10 | 15 | 15 | 30 |
产生沉淀的质量(g) | 1.97 | 3.94 | 3.94 | X |
表中第__________次反应恰好完全进行
(5)请计算样品中氢氧化钠的质量分数?__________(请写具体解题过程)