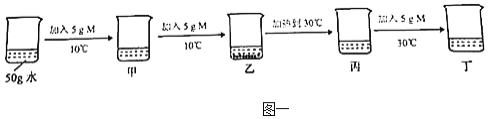
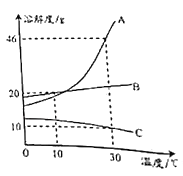
题目内容
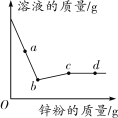
【题目】根据下图所示信息进行计算。假设:稀硫酸转移完全且生成气体全部逸出。
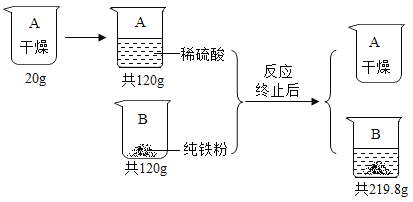
(1)生成H2的质量为_____________g。
(2)反应后的溶液中溶质质量分数为多少?(写出解题过程,最后结果保留两位小数)
【答案】(1)0.2g; (2)
【解析】根据题中提供的数据可知,(1)生成氢气的质量为120g+100g--219.8g=0.2g;
(2)设生成硫酸亚铁的质量为x,参加反应的铁的质量为Y
Fe + H2SO4 === FeSO4 + H2↑
56 152 2
X y 0.2g
56/x=2/0.2g 152/y= 2/0.2g
X=5.6g y= 15.2g
溶液的总质量为:5.6g+100g-0.2g=105.4g
(2)反应后的溶液中溶质质量分数为15.2g/105.4g×100%=14.42%

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的舞台。大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒中的乙醇生成乙酸乙酯。下表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为 _______;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为_______(计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X的化学式为________。
【题目】下列化学方程式及其反应类型都正确的是
选项 | 化学方程式 | 反应类型 |
A | Mg+O2 | 化合反应 |
B | H2O2 | 分解反应 |
C | Fe+H2SO4=FeSO4+H2↑ | 置换反应 |
D | 2KNO3+Ba(OH)2=Ba(NO3)2+2KOH | 复分解反应 |
A.AB.BC.CD.D