题目内容
质量守恒定律的定量研究对化学科学发展具有重大作用.(1)用化学方法可将过度排放的二氧化碳“变废为宝”.在一定条件下,二氧化碳和氢气可实现以下转化:CO2+H2
 X+H2O,其中X的化学式为 .
X+H2O,其中X的化学式为 .(2)如图为某化学反应的微观模拟图,“
 ”和“
”和“ ”分别表示不同元素的原子:
”分别表示不同元素的原子:由“
 ”聚集成的物质 (填“可能”或“不可能”)是氧化物,参加反应的两种反应物分子“
”聚集成的物质 (填“可能”或“不可能”)是氧化物,参加反应的两种反应物分子“ ”与“
”与“ ”的个数比为 .
”的个数比为 .(3)相同的反应物,若其质量比不同,可能发生不同的化学变化.例如:C+O2
 CO2(氧气充足),2C+O2
CO2(氧气充足),2C+O2 2CO(氧气不足);已知1mol碳充分燃烧放出393.5千焦的热量,不充分燃烧(生成CO)放出110.5千焦的热量.由上可知,煤燃烧不充分引发的弊端有 .
2CO(氧气不足);已知1mol碳充分燃烧放出393.5千焦的热量,不充分燃烧(生成CO)放出110.5千焦的热量.由上可知,煤燃烧不充分引发的弊端有 .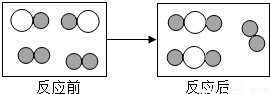
【答案】分析:(1)根据质量守恒定律进行解答;
(2)观察微观模拟图,总结构成物质的基本微粒,找出化学反应中各物质的粒子个数关系;
(3)由煤不充分燃烧会产生CO污染环境,而且放热少.
解答:解:(1)根据质量守恒定律,化学反应前后元素的种类和原子的个数不变,反应前C:1、H;2、O:2,反应后H:2、O:1,故X的化学式为:CO;
(2)将图中前后无变化的微粒去除得图:
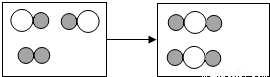 ,
,
图示表示 由“ ”聚集成的物质由两种元素组成,可能一种为氧元素,所以该物质可能为氧化物;“
”聚集成的物质由两种元素组成,可能一种为氧元素,所以该物质可能为氧化物;“ ”与“
”与“ ”的个数比为,两种反应物分子个数比为2:1;
”的个数比为,两种反应物分子个数比为2:1;
(3)由题干可知,煤燃烧不充分会污染环境,产生有毒气体CO;二是放热少,浪费能源;
故答案为:
(1)CO;
(2)可能;2:1;
(3)其一:污染环境(产生有毒CO,污染环境);其二:浪费能源(放出热量少).
点评:本题主要考查了物质的微观构成和宏观组成等方面的内容,难度不大
(2)观察微观模拟图,总结构成物质的基本微粒,找出化学反应中各物质的粒子个数关系;
(3)由煤不充分燃烧会产生CO污染环境,而且放热少.
解答:解:(1)根据质量守恒定律,化学反应前后元素的种类和原子的个数不变,反应前C:1、H;2、O:2,反应后H:2、O:1,故X的化学式为:CO;
(2)将图中前后无变化的微粒去除得图:
 ,
,图示表示 由“
 ”聚集成的物质由两种元素组成,可能一种为氧元素,所以该物质可能为氧化物;“
”聚集成的物质由两种元素组成,可能一种为氧元素,所以该物质可能为氧化物;“ ”与“
”与“ ”的个数比为,两种反应物分子个数比为2:1;
”的个数比为,两种反应物分子个数比为2:1;(3)由题干可知,煤燃烧不充分会污染环境,产生有毒气体CO;二是放热少,浪费能源;
故答案为:
(1)CO;
(2)可能;2:1;
(3)其一:污染环境(产生有毒CO,污染环境);其二:浪费能源(放出热量少).
点评:本题主要考查了物质的微观构成和宏观组成等方面的内容,难度不大

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: 由“
由“ ”聚集成的物质
”聚集成的物质 质量守恒定律的定量研究对化学科学发展具有重大意义.
质量守恒定律的定量研究对化学科学发展具有重大意义. ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: ”聚集成的物质
”聚集成的物质 ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: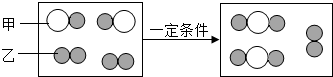
 ”聚集成的物质
”聚集成的物质