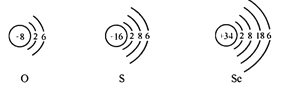
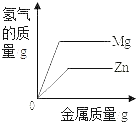
题目内容
【题目】甲、乙两同学进行如图①所示的实验(已知: CaCl2+Na2CO3===CaCO3↓+2NaCl)。实验结束后,丙同学把A、B两支试管中的物质倒入烧杯C中(如图②), 充分混合后发现白色沉淀明显增多。
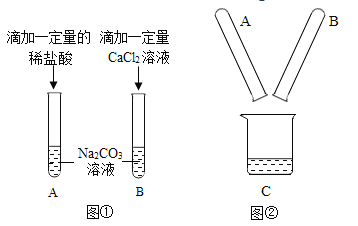
(1)充分反应后,试管A中剩余的反应物是_______(填“HCl”或“Na2CO3”)。
(2)烧杯C中的溶质有可能是________(填字母序号)。
A. NaCl、Na2CO3 B.NaCl、CaCl2 C.NaCl D. CaCl2
【答案】Na2CO3ABC
【解析】
(1)实验结束后,把A、B两支试管中的物质倒入同一洁净的烧杯中,充分混合后发现白色沉淀明显增加,说明A中反应后碳酸钠过量,B中氯化钙过量,因此甲同学的实验完成后,A试管一定有剩余的物质是碳酸钠;(2)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳;碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,因此溶质一定有氯化钠,混合后碳酸钠与氯化钙两者那个过量,溶液中还会有那个,故选ABC。

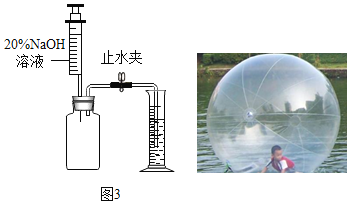
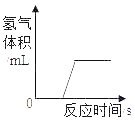
【题目】某研究性学习小组在”利用燃碳法测定空气中氧气的体积分数”的实验时(如图),发现个现象:用氢氧化钠溶液吸收生成的二氧化碳后,进入氧气瓶中水的体积分数仍然小于1/5。

(提出问题)是什么原因导致测量不准确呢?
(猜想与假设)他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气。
(探究一)
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为_____同学的猜想不合理。
(查阅资料)木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达14.0%,8.0%和16.0%
(进行实验)乙同学又利用上述装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验讨论 |
①将足量木炭点燃,迅速插入集气瓶中 | _____ | 木炭燃烧没有消耗完集气瓶中的氧气 |
②待装置冷却后,将燃着的________(填“棉花”或蜡烛)再伸入集气瓶中 | _____ |
(实验反思)小明从木炭燃烧产物的角度猜想还可能是生成了_____导致测量结果小于1/5;于是用注射器抽取集气瓶内的气体做了图2所示的实验,当观察到澄清石灰水变浑浊,可证明小明的猜想成立,则该现象涉及的化学方程式为_____,该实验中没有观察到氧化铜粉末变红的原因可能是_____
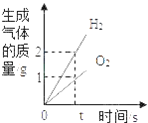
(拓展迁移)若要测量“水上步行球”内空气中二氧化碳的体积含量,利用图3装置,若集气瓶中收集的“水上步行球”内空气样品的体积为500mL,加入足量的氢氧化钠溶液充分振荡后,打开止水夹后量筒中的水流入集气瓶中5mL,则球内空气中CO2的体积含量是_____