��Ŀ����
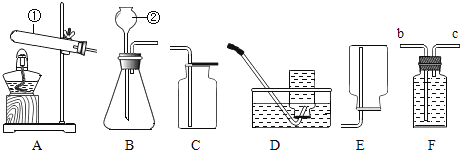
����Ŀ����ͼ����A��B��C���ֹ������ʵ��ܽ������ͼ��
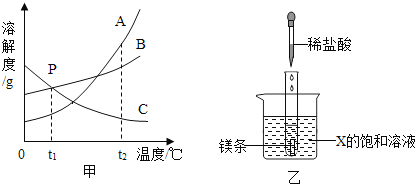
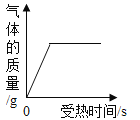
��1����ͼ�У�t2��ʱ��A��B��C���������У��ܽ��������___________��P������ʾ�ĺ���Ϊ_________________________ ��
��2��t1��ʱ����C���ʵIJ�������Һת��ɱ�����Һ�ɲ�ȡ�ķ�����___________ , ___________________��
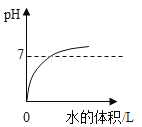
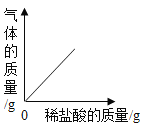
��3������ͼ��ʾ��20��ʱ�����Թܷ���ʢ��X�ı�����Һ���ձ��У����Թ��м���þ�����ټ���������ϡ���ᣬ��Ӧ����ʽΪ__________________________����ʱ�ձ��г��ֻ��ǣ���X����ΪA��B��C���ֹ��������е���Щ��_____________________��
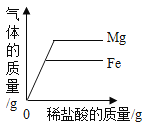
��4����t1��ʱA��B��C�������ʱ�����Һ���¶����ߵ�t2��ʱ��������Һ���������������ɴ�С��ϵ��_______________________��
���𰸡�A ��t1��ʱ��C��B�����ʵ��ܽ����� �������� �����ܼ� Mg+2HCl=MgCl2+H2�� C B>A>C
��������
��1����ͼ�У�t2��ʱ��A��B��C���������У��ܽ��������A��P������ʾ�ĺ���Ϊ����t1��ʱ��B��C���ܽ����ȣ�
��2��t1��ʱ����C���ʵIJ�������Һת��ɱ�����Һ�ɲ�ȡ�ķ����У��������ʡ������ܼ���
��3��þ�����ᷴӦ�����Ȼ�þ����������Ӧ����ʽΪMg+2HCl=MgCl2+H2������Ӧ���ȣ��ձ��г��ֻ���˵���ܽ�����¶����߶���С��C���ܽ�����¶ȵ����߶����٣���X��C��
��4����t1��ʱA��B��C�������ʱ�����Һ���¶����ߵ�t2��ʱ��������Һ���������������ɴ�С��ϵ��B��A��C����Ϊ���º�A��B�������������䣬C������������С��

����Ŀ��ij�����õ�ⱥ��ʳ��ˮ�ķ��������������ռ�����Ȼ�����Ʒ����Ӧ�Ļ�ѧ����ʽ��2NaCl+2H2O![]() 2NaOH+H2��+Cl2���������ֹ�ҵ��Ϊ���ȼҵ����ij�о���ѧϰС��Ըó��������ռ���Ʒ��������̽����
2NaOH+H2��+Cl2���������ֹ�ҵ��Ϊ���ȼҵ����ij�о���ѧϰС��Ըó��������ռ���Ʒ��������̽����
��������⣩�ռ���Ʒ�п��ܺ�����Щ���ʣ�
�����룩
����1�����ܺ���Na2CO3��
����2�����ܺ���NaCl��
����3�����ܺ���_____��
��������1��������_____ ���û�ѧ����ʽ��ʾ����
�����ʵ�飩
ʵ�鲽�� | ʵ������ | ���ͻ���� |
I��ȡ�����ռ���Ʒ�����Թ��У���ˮ�ܽ⣬�����ִ����Թ���ڡ� | �Թ���ڷ��� | ԭ����_____�� |
II����I���õ���Һ����μ��� ϡ���������� | �տ�ʼ_____��һ��ʱ��������ʹ����ʯ��ˮ����ǵ����塣 | ����1���ܳ����� |
III����II���õ���Һ��_____�� | ������ɫ���� | ���ʵ��II������3������ |
�����������ۣ�
С��ͬѧ�����������ʵ��II��ϡ����Ҳ������ϡ������桱������Ϊ���Ĺ۵�_____�����ȷ������ȷ������������_____��
����Ŀ��С���Ӻ�������һЩǶ��ɳ���ı��ǣ���Ҫ�ɷ�Ϊ̼��ƣ���Ϊ�ⶨ̼��Ƶĺ��������������µ�ʵ�飺���ȣ���ȡ50g������Ʒ��Ȼ��200g�����5�μ��루�������ʾ��������ᷴӦ��Ҳ������ˮ����ʵ������е����ݼ�¼���±���
ϡ��������/g | 40 | 40 | 40 | 40 | 40 |
ʣ���������/g | 40.0 | X | 20.0 | 10.0 | 5.0 |
��1��x=_____g
��2��С����ñ�����Ʒ��̼��Ƶ�����������_____��
��3�������������ʵ���������Ϊ________������ȷ��0.1%��
��4���������ɵĶ�����̼�ռ����������ж��ٿˣ�________________