题目内容
【题目】如图是实验“使水沸腾的冰”。在平底烧瓶中加入一定量的水,加热使水沸腾后停止加热。用胶塞塞住瓶口,将烧瓶倒转过来,这时水已经停止沸腾了,此时在平底烧瓶的底部放上一层冰块,就可以观察到烧瓶里的水又重新沸腾了,请完成下列各题:
(1)水重新沸腾的原因是________;
(2)电解水时,检验正极气体的方法是_________;
(3)写出电解水实验反应的化学方程式__________。
【答案】瓶内温度降低,水蒸气液化,气体压强减小,因为水的沸点会随气压的减小而降低 将带火星的木条伸入产生的气体中,观察木条是否复燃 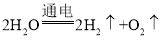
【解析】
(1)在平底烧瓶的底部放上一层冰块,瓶内温度降低,水蒸气液化,气体压强减小,因为水的沸点会随气压的减小而降低,因此水会重新沸腾起来;
(2)电解水负极生成的是氢气,正极生成的是氧气,生成的氢气和氧气的体积比是2:1。氧气能使带火星的木条复燃。检验正极气体的方法是将带火星的木条伸入产生的气体中,观察木条是否复燃;
(3)水电解生成氢气、氧气,该反应的化学方程式为: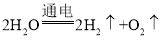 。
。

【题目】化学小组同学利用下图装置分别完成2个实验。
序号 | 甲 | 乙 | 分液漏斗 |
1 | 大理石 | 澄清石灰水 | 稀盐酸 |
2 | 二氧化锰 | 80℃热水及一小块白磷 | 过氧化氢溶液 |

(1)实验1:打开b和a,将分液漏斗中过量的盐酸注入,关闭a,此时乙中反应的化学方程式是_____,一段时间后,关闭b,观察到乙中液体变澄清,产生此现象的原因是_____。
(2)实验2:观察到乙中白磷的现象是_____;打开b和a,当分液漏斗中的过氧化氢溶液全部注入后,关闭a,观察到乙中白磷的现象是_____。关闭b,一段时间后,白磷的现象及原因是_____。
【题目】合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于其中任何一个组成金属的熔点。下表是一些金属熔点的数据。
金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
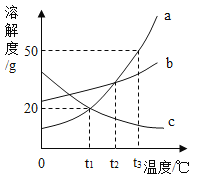
(1)铅锡合金中某种金属的质量分数与合金的熔点有如如图所示的关系,其中横坐标表示的是________的质量分数;当合金熔点最低时,合金中铅与锡的质量比为____________。
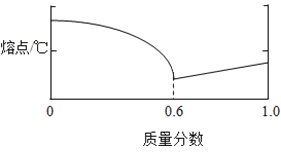
(2)保险丝由铋、铅、锡、镉等金属组成,其熔点约为________。
A.20-40℃ B.60-80℃ C.230-250℃ D.300-320℃
(3)青铜器的主要成分是铜锡合金。崭新的青铜器呈土黄色。当青铜器长期埋在地下,逐渐形成了绿色的铜绿(主要成分Cu2(OH)2CO3),从其化学式可知,铜绿是铜与___________、___________和___________(填物质的化学式)长期作用的结果。
(4)通常情况下铁的合金制品也比较容易生锈,请写出工业上用稀盐酸除去铁锈(Fe2O3)的化学方程式_______________________________。
【题目】制笔行业中经常用到铂、钌(Ru)等贵金属。现有 5 种含钌元素的物质:Ru、RuO2、Ru2O3、RuCl3、K2RuO4。回答下列问题:
(1)RuO2 读作__________。
(2)上述 5 种物质中钌元素的化合价一共有_________种。
(3)从物质分类角度来看,K2RuO4 属于_________。(填选项)
A.化合物 | B.氧化物 | C.碱 | D.盐 |
(4)H2 与 Ru2O3 在加热条件下反应可得到 Ru。写出反应的化学方程式 。