题目内容
【题目】如图所示是医院常用的药瓶和注射器,请你据图回答:
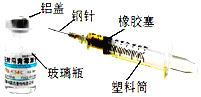
(1)含有金属材料的是______(写一种即可,下同)。
(2)注射器洗净后可以用于家庭小实验,可以代替______仪器使用。
(3)钢针一般用不锈钢制造,主要是由于其不容易生锈,请你写出生活中防止铁制品生锈的方法(一条即可)______。
(4)请写出工业炼铁的主要反应原理的化学方程式(以一氧化碳还原氧化铁为例):______。
(5)铝具有很好的抗腐蚀性能,原因是______(用化学方程式表示)。
(6)铝的金属活性比铁强,请写出铝放入硫酸亚铁溶液中反应的化学方程______。
(7)在AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,充分反应后过滤,得滤渣和滤液。
①若滤液呈无色,则滤渣中一定含有的物质是______ (填化学式);
②若向滤渣中滴加稀盐酸,有气泡产生,则滤液中溶质的成分是______。
【答案】钢针; 量筒或滴管; 保持铁制品表面的洁净和干燥; 3CO+Fe2O3![]() 2Fe+3CO2; 4Al+3O2═2Al2O3; 2Al+3FeSO4═Al2(SO4)3+3Fe。 Cu、Ag; Zn(NO3)2。
2Fe+3CO2; 4Al+3O2═2Al2O3; 2Al+3FeSO4═Al2(SO4)3+3Fe。 Cu、Ag; Zn(NO3)2。
【解析】
(1)金属材料包括纯金属以及它们的合金,所以使用的金属材料是铝箔、钢针;
(2)生活中用注射器可以控制液体的滴加速度并且注射器上有刻度,所以注射器可以代替胶头滴管、分液漏斗、量筒等;
(3)铁生锈的条件是铁和氧气、水同时接触,所以生活中防止铁制品生锈的方法保持铁制品表面的洁净和干燥;
(4)一氧化碳能与氧化铁高温反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(5)通常情况下,铝和氧气反应的化学方程式为:4Al+3O2═2Al2O3。
(6)铝和硫酸亚铁溶液反应生成铁和硫酸铝,反应的化学方程式2Al+3FeSO4═Al2(SO4)3+3Fe。
(7)①在金属活动性顺序中,锌>氢>铜>银,锌先与硝酸银反应生成硝酸锌和银,后与硝酸铜反应生成硝酸锌和铜,若滤液呈无色,说明滤液中无铜离子,那么硝酸银一定被反应完全,硝酸铜也被反应完全,则滤渣中一定含有的物质是Cu、Ag;②在滤渣中加入盐酸有气体产生,则一定含有锌,说明加入的锌粉过量,在AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粉,锌与硝酸银反应生成硝酸锌和银,和硝酸铜反应生成硝酸锌和铜,生成的铜会与硝酸银反应生成硝酸铜和银,滤液中溶质为Zn(NO3)2。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】某无色气体可能由CO和H2中的一种或两种组成,为了确定其成分,化学兴趣小组的同学进行了以下探究。
(查阅资料)白色的无水硫酸铜遇水会变成蓝色。
(实验设计)
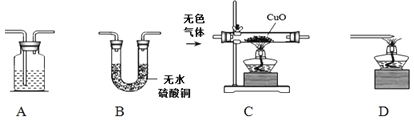
①如图装置A中盛放的液体名称是_____。
②如图装置的正确连接顺序是:_____(填字母,且每套装置限用一次)。
(实验猜想)若装置连接正确,有关无色气体成分的猜想和对应的实验现象如下表:
无色气体的成分 | 对应的实验现象 | ||
装置A中的液体 | 装置B中的固体 | 装置C中的固体 | |
猜想一:只有CO | 变浑浊 | 无明显现象 | 变红 |
猜想二: | 变浑浊 | 变蓝 | |
猜想三:只有H2 | _____ | _____ | |
(实验结论)进行实验,证明猜想二正确。
(拓展延伸)铁元素可以形成三种氧化物,分别是Fe2O3、Fe3O4和FeO(黑色)。将CuO改换为铁的氧化物粉末(可能由一种或几种铁的氧化物组成),仍用上图装置按原连接顺序进行实验,通过测定装置A、B在反应前后的质量变化进行计算分析,从而判断出该氧化物的组成。实验前,装置C需做的一处改进是_____。要证明该黑色粉末的组成,最简单的方法只需用磁铁吸引并观察粉末颜色即可(已知Fe3O4具有磁性,可被磁铁吸引)。
(1)为了防止粉末吸在磁铁上难以快速方便地取下,应_____(填写一种方法)。
(2)若粉末全部能被磁铁上全部吸引,则该粉末只有Fe3O4。
(3)若磁铁上有黑色粉末,且_____,则该粉末含有FeO、Fe3O4。
(4)若磁铁上有黑色粉末,且剩余粉末并非完全的黑色,则该粉末含有_____种成分。
【题目】金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。

实验编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
20% | 锌粒 | 31.7 | |
20% | 锌片 | 50.9 | |
30% | 锌粒 | 61.7 | |
30% | 锌片 | 79.9 |
(1)小组同学用右图装置收集并测量氢气的体积,其中量筒的作用是 ,氢气应从 (填e或f或g)管通入。(已知:氢气难溶于水)
【收集证据】
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 。
【得出结论】
(3)结论是 。
【评价与反思】
(4)下表是小组同学第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应快慢的变化 ,并解释第二分钟以后变化的原因 。
(5)锌与硫酸反应的快慢可能还受温度因素的影响,请设计实验验证 。