题目内容
用不纯的锌与稀硫酸反应能加快产生氢气的速率,实验室用13g锌粉和5g铜粉混合物与足量的稀硫酸反应,可产生多少克的氢气?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据金属的活动性顺序可以知道锌和稀硫酸反应,而铜不反应,所以可以根据锌粉的质量进行求算.
解答:解:铜不能与硫酸反应,能产生氢气的只有锌粉与稀硫酸的反应.
设生成氢气质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
13g x
=
x=0.4g
答案:可生成氢气0.4g.
设生成氢气质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
13g x
| 65 |
| 13g |
| 2 |
| x |
x=0.4g
答案:可生成氢气0.4g.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景等,结合所学的相关知识和技能,细致地分析题意等各种信息资源,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
向含AgNO3、Cu(NO3)2、Mg(NO3)2混合溶液中,加入一定量的锌粒,充分反应后过滤,对滤液和滤渣的描述不可能的是( )
| A、滤渣中含有Ag,滤液中溶质为Cu(NO3)2、Mg(NO3)2 |
| B、滤渣中含有Ag、Cu,滤液中溶质为Cu(NO3)2、Zn(NO3)2、Mg(NO3)2 |
| C、滤渣中含有Ag、Cu、Zn,滤液中含有Zn(NO3)2、Mg(NO3)2 |
| D、滤渣中含有Ag,滤液中溶质为AgNO3、Cu(NO3)2、Zn(NO3)2、Mg(NO3)2 |
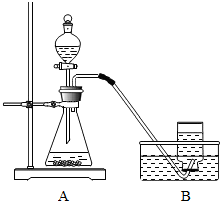 某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.
某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.