题目内容
【题目】下图是配制50g质量分数为15% 的氯化钠溶液的操作过程示意图,试回答:
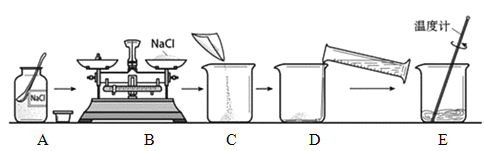
(1) 上述操作过程示意图中的错误有________ 处,还缺少一个操作步骤是_________。
(2) B操作中实际称量氯化钠的质量是_______ g。(说明:1g以下用游码)
(3) D操作应选用 __________ 的量筒(从10 mL、50 mL 、100 mL中选择);量水时,量筒必须平放,视线要跟量筒中水的凹液面的 _______________处保持水平。
(4)E操作的后果是 ____ ,E操作的目的是_______________。
(5)若B的操作是正确的。下列的错误操作可能导致溶液溶质质量分数小于15%的是___________ (填序号)。
① C操作中有固体洒落 ② D操作中有少量水溅出
③ E操作中有少量溶液溅出 ④ 量取水时,仰视读数
(6)实验结束后,要对玻璃仪器进行洗涤。玻璃仪器洗涤干净的标准是____________。
【答案】 3 装瓶贴标签 6.5 50mL 最低 易将温度计的水银球损破,从而污染溶液 加快溶解 ①④ 洗过的玻璃仪器内壁附着的水既不成水滴,也不成股流下时,表示玻璃仪器已经洗干净
【解析】(1)观察图示的操作,并据正确操作和配制溶液的步骤分析解答;(2)依据物码倒置的计算方法分析;(3)计算配制溶液时所需要水的量选择适合的量筒;并说明量筒的正确使用方法;(4)温度计易将温度计的水银球损破,从而污染溶液;搅拌说明操作对于配制溶液所起的作用;(5)溶液溶质质量分数小于15%可能是溶质偏小,或溶剂质量偏大;(6)依据玻璃仪器洗涤干净的标准回答。(1)A操作中瓶塞应倒放,B操作称量时应左物右码,E操作中不应用玻璃棒搅拌,故错误有三处,还缺少一个操作步骤是装瓶贴标签;(2)要配制50g质量分数为15%的氯化钠溶液,需要氯化钠的质量为50g×15%=7.5g,根据题意,1g以下用游码,故正确称量方法是加7g砝码,游码拨到0.5g刻度处;B操作中物码倒置时,称量物的质量=砝码的质量-游码的质量,故实际称量氯化钠的质量是7g-0.5g=6.5g;(3)应量取水的质量是50g-7.5g=42.5g,水的密度是1g/cm3,故需水47.5mL,因此需要选择50mL量筒;在使用量筒量取液体时,为准确量取,应保持视线与凹液面的最低处保持水平;(4)E操作的后果是易将温度计的水银球损破,从而污染溶液;用玻璃棒搅拌是为加快固体食盐的溶解;(5)所取食盐质量偏小或所取水的体积偏大是导致所配制溶液的溶质质量分数偏低的两个原因。若B操作正确,① C操作有固体洒落会导致所取溶质偏小,溶质质量分数偏小,正确;② D操作中有少量水溅出,导致水的体积偏小,溶质质量分数偏大,错误;③ E操作中有少量溶液溅出对溶质的质量分数无影响,错误;④量取水时采取仰视而导致所取水的体积偏大,溶质质量分数偏小,正确。故选①④;(6)玻璃仪器洗涤干净的标准是:洗过的玻璃仪器内壁附着的水既不成水滴,也不成股流下。

 阅读快车系列答案
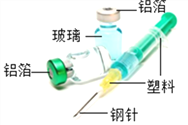
阅读快车系列答案【题目】央视频道《是真的吗?》栏目中有一段视频:将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,某同学取“锡纸”进行了以下探究:
探究一:“锡纸”燃烧的原因
“锡纸”两端接入电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件分析:开始“锡纸”不燃烧但短路后却能燃烧的原因是___________。
探究二:“锡纸”中金属的成分
【提出问题】“锡纸”中的金属是锡吗?
【查阅资料】①“锡纸”是锡箔或铝箔
②锌粉是一种深灰色固体
③锡(Sn)与酸或与某些金属化合物溶液反应生成+2价锡的化合物
【提出猜想】猜想Ⅰ:“锡纸”中的金属是锡 猜想Ⅱ:“锡纸”中的金属是铝
【进行实验】设计方案并进行实验
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 | 根据实验现象,结合金属活动性顺序 可知猜想___(填“Ⅰ”或“Ⅱ”)成立; 反应的化学方程式为______________ |
【交流讨论】
(1)实验中打磨“锡纸”的目的是_______________
(2)下列物质的溶液可以替代氯化锌溶液完成上述实验的是___填字母序号).
A.氯化铜 B.硝酸银 C.硫酸钠 D.硫酸亚铁
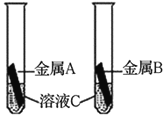
【拓展应用】证明铁、铜、银三种金属活动性顺序的实验方案如下,请将内容补充完整。
C是__________________ 溶液。
实验操作 | 实验现象 | 实验结论 |
| _____________ | 铁、铜、银三种金属的活动性顺序是:Fe>Cu>Ag |