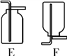题目内容
【题目】铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。铁是生产、生活中应用很广泛的一种金属。下列是与铁的性质有关的部分实验图,请回答下列问题。
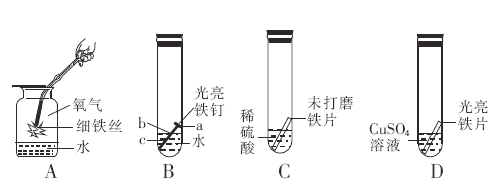
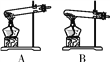
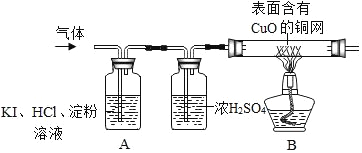
(1)A中铁丝在氧气中燃烧,为什么要预留一层水______。
(2)在空气中__制品(填“铝”或“铁”)更耐腐蚀。
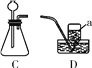
(3)B中铁钉最易生锈的部位是 ___(填“a”“b”或“c”)。
(4) C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学
方程式是__________。
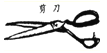
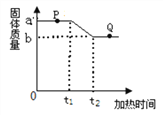
(5)D中反应一段时间后,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反
应前相比____(填“增大”“不变”或“减小”)。
(6)某化学小组向AgNO3,和Al(N03)3的混合溶液中加入一定量的铜、锌混合粉末,充分
反应后过滤,得到滤渣和滤液。
①滤液为无色溶液,则滤渣中一定含的物质是___。
②若向滤渣中滴加盐酸有气泡产生,则滤液中一定含有的溶质是___。
【答案】 防止高温熔融物炸裂瓶底 铝 b Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 减小 银、铜 硝酸铝、硝酸锌
【解析】(1)铁在氧气中剧烈燃烧,放出大量的热量,为了防止高温熔融物炸裂瓶底,需要在瓶底放置少量的水;
(2)铝的化学性质比铁活泼,但铝易与空气中的氧气反应生成致密的氧化铝保护膜,故铝制品更耐腐蚀;
(3)B中b点处铁钉既与水接触又与氧气接触,故b点最易生锈;
(4)C中刚开始是铁钉表面的氧化铁与稀硫酸反应生成硫酸铁和水,反应方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(5)D中是铁与硫酸铜的反应,固体表面减少了铁,增加了铜,铜的相对原子质量大于铁的相对原子质量,故固体的质量增加,溶液中减少是铜离子,增加了铁离子,故溶液的质量减少;
(6)①向AgNO3,和Al(N03)3的混合溶液中加入一定量的铜、锌混合粉末,滤液为无色溶液,说明铜没有发生反应,只有锌发生反应,会先置换出银,锌有可能刚好完全反应,故滤渣中一定有银、铜;
②锌能置换出银,不能置换出铝,若向滤渣中滴加盐酸有气泡产生,说明加入的锌是过量的,因为银和铜都不能与酸反应放出氢气,说明溶液中没有硝酸银,故溶液中有未反应的硝酸铝和生成的硝酸锌;