题目内容
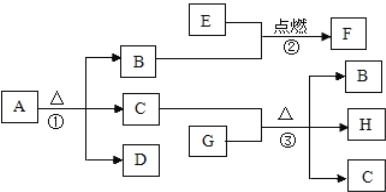
【题目】实验与探究是进行化学学习的一种重要方式,以“碳和碳的化合物”进行以下探究。
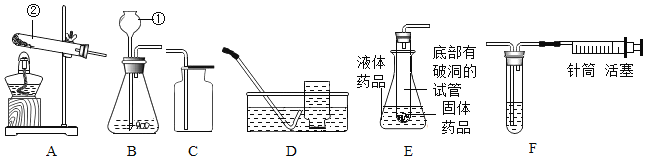
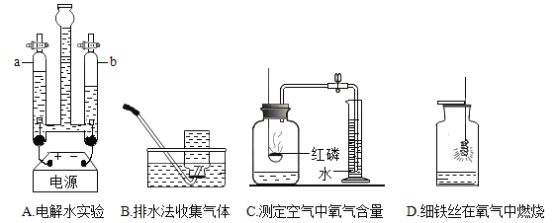
(1)利用如图装置可进行气体性质的探究实验(导管a处用火柴点燃)
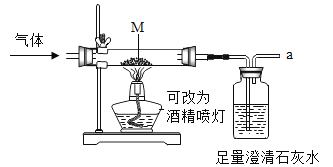
Ⅰ.探究CO与CuO的反应:通入气体一氧化碳,M处为氧化铜,加热前先通一氧化碳的目的是_____;M处反应的化学方程式为_____;澄清石灰水的作用是_____。
Ⅱ.探究CO2与C的反应(改为酒精喷灯):通入气体二氧化碳,M处为木炭,观察到玻璃管中的现象是_____,M处反应的化学方程式为_____。导管a处点燃的目的是_____。
(2)化学小组取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究。
(提出问题)剩余固体成分是什么?
(猜想与假设)
猜想一:_____。
猜想二:是氧化钙与碳酸钙的混合物。
(实验探究)
实验步骤 | 实验现象 | |
步骤1 | 取一定量的剩余固体于试管中,加入一定量的水,振荡、静置。取上层清液,滴加无色酚酞试液。 | _____ |
步骤2 | 另取一定量的剩余固体于试管中,加入足量_____。 | 有气泡产生 |
(探究结论)通过探究,猜想二成立。
【答案】排出装置中的空气 CuO+CO![]() Cu+CO2 检验二氧化碳 固体减少 C+CO2
Cu+CO2 检验二氧化碳 固体减少 C+CO2![]() 2CO 防止一氧化碳扩散到空气中污染环境 是氧化钙 溶液变红色 稀盐酸
2CO 防止一氧化碳扩散到空气中污染环境 是氧化钙 溶液变红色 稀盐酸
【解析】
加热条件下氧化铜和一氧化碳反应生成铜和二氧化碳,高温条件下二氧化碳和碳反应生成一氧化碳,一氧化碳有毒,扩散到空气中污染环境;
碳酸钙在高温条件下分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙溶液显碱性,能使酚酞试液变红色;
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
(1)Ⅰ.加热前先通一氧化碳的目的是排出装置中的空气,以防止发生爆炸;M处氧化铜和一氧化碳反应生成铜和二氧化碳,反应的化学方程式为:CuO+CO![]() Cu+CO2;
Cu+CO2;
澄清石灰水的作用是检验二氧化碳;
Ⅱ.观察到玻璃管中固体减少,直至消失,是因为M处碳和二氧化碳反应生成一氧化碳,反应的化学方程式为:C+CO2![]() 2CO;导管a处点燃的目的是防止一氧化碳扩散到空气中污染环境;
2CO;导管a处点燃的目的是防止一氧化碳扩散到空气中污染环境;
(2)[猜想与假设]猜想一:碳酸钙完全反应后是氧化钙;猜想二:碳酸钙部分反应后是氧化钙与碳酸钙的混合物;
[实验探究]氧化钙能和水反应生成氢氧化钙,氢氧化钙溶液显碱性,能使酚酞试液变红色;
加入足量稀盐酸,产生气泡,是因为碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。