题目内容
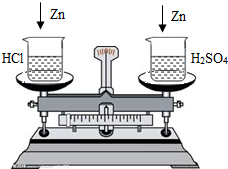
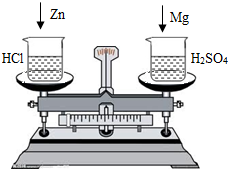
在托盘天平的两边各放一只烧杯,调节至平衡.在两只烧杯中分别注入相同质量的稀硫酸和稀盐酸,然后再向左盘的稀硫酸和右盘的稀盐酸中分别投入相同质量的镁条和锌粒,当镁条和锌粒都完全溶解后,天平指针( )
| A、偏左 | B、偏右 | C、居中 | D、无法判断 |
分析:反应物放在一起不反应的状态时,天平是平衡的,指针的偏转主要是看生成氢气的多少,因此解题时判断氢气多少则成为解题的关键所在.
解答:解:锌粒和镁条全部溶解,说明酸足量,设金属的质量为65,镁生成的氢气质量为y
Zn+2HCl═ZnCl2+H2↑
65 2
生成的氢气是2
Mg+H2SO4═MgSO4+H2↑
24 2
65 y
=
y=5.4
镁生成的氢气多,指针偏右
故选B
Zn+2HCl═ZnCl2+H2↑
65 2
生成的氢气是2
Mg+H2SO4═MgSO4+H2↑
24 2
65 y
| 24 |
| 2 |
| 65 |
| y |
y=5.4
镁生成的氢气多,指针偏右
故选B
点评:本题考查了金属与酸反应生成氢气质量的关系,完成此题,可以依据反应的化学方程式,从酸的质量和金属的质量的角度进行.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目