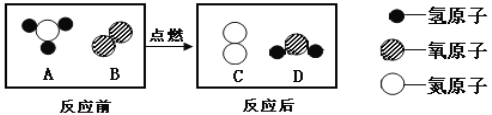
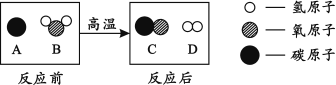
��Ŀ����
����Ŀ����CuSO4��Һ�м���һ����NaHCO3��Һ���۲쵽�����ݲ���������ɫ���塣
��һ��������ͨ����������ʯ��ˮ��ʯ��ˮ����ǣ�����Ϊ_____��
�������������
�����룩��������Ǣ�Cu(OH)2��CuCO3��CuCO3��Cu(OH)2�Ļ����
�����ϣ�CuCO3��Cu(OH)2���Ⱦ���ֽ����ɶ�Ӧ������������,��ˮCuSO4��ˮ����
��ʵ�飩�������õ����������������ɫ���塣
��1��ȡ�������壬����_____��Һ���������ݣ���²�ٲ�������
��2����ȡ�������壬��ּ��ȣ�������������ʹ��ˮCuSO4��������²�_____��ѡ������������������������
�����죩����⣬�ù���ΪxCu(OH)2��yCuCO3��zH2O��С��ͬѧ��ȡ24.0g���壬����ʦ��ָ���½�������ʵ�飬ȷ��������ɣ�
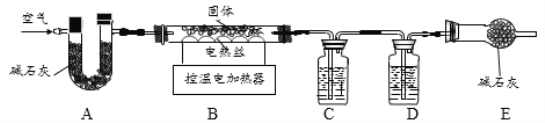
��3��ʵ��ǰ������Ҫ_____��
��4��װ��C��D�ֱ��������ɵ����壬��D�����ʢ��_____��������ĸ��
a.����ʯ��ˮ b.Ũ���� c.Ũ����������Һ
��5��B�з�Ӧ��ȫ��Ҫͨ��һ��ʱ�������Ŀ����_____��
��6��ʵ����C����3.6g��D������4.4g����x:y:z=_____��
���𰸡�CO2 ϡHCl �� ���װ�õ������� c ʹ���������屻��ȫ���� 1:1:1
��������
��һ��������ͨ����������ʯ��ˮ��ʯ��ˮ����ǣ������Ƕ�����̼��
������[ʵ��]
��1��ȡ�������壬����ϡ���ᣬ�������ݣ�˵�������к���̼��ͭ����²�ٲ�������
��2����ȡ�������壬��ּ��ȣ�������������ʹ��ˮCuSO4����������Ϊ������ͭ�ֽ�������ˮ��������к���������ͭ���²�۳�����
��3������������μӻ����ɵ�ʵ�飬ʵ��ǰ������Ҫ���װ�������ԣ�
��4��װ��C��D�ֱ��������ɵ����壬��������ˮ�����Ͷ�����̼����D�����ʢ��Ũ����������Һ���������ն�����̼����ѡc��
��5��B�з�Ӧ��ȫ��Ҫͨ��һ��ʱ�������Ŀ���ǽ�������װ�������ɵ�ˮ�Ͷ�����̼����C��Dװ���У�ʹ���������屻��ȫ���գ�
��6��ʵ����C����3.6g��˵����Ӧ������3.6gˮ��D������4.4g��˵����Ӧ������4.4g������̼��
��Ӧ��������ͭ����Ϊ��24.0g��3.6g��4.4g��16g
��̼��ͭ����Ϊx����������ͭ����Ϊy��

![]()
x��12.4g
y��8g
������ͭ�ֽ���������ͭ����Ϊ��16g��8g��8g
��������ͭ����Ϊm����Ӧ����ˮ������Ϊn��

![]()
m��9.8g
n��1.8g
�ᾧˮ����Ϊ��3.6g��1.8g��1.8g
����������![]() ��x��y��z
��x��y��z
��x��y��z��1��1��1

����Ŀ��ȡ50g̼���ƺ��Ȼ��ƵĻ����Һ����������μ���ϡ���ᡣ����ϡ���������������������������±���������ܽ�Ⱥ��Բ��ƣ���
��һ�� | �ڶ��� | ������ | |
ϡ���������/g | 20 | 40 | 60 |
�������������/g | 2.0 | m | 5.5 |
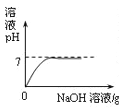
��ȡ�û����Һ50g��������Ũ�ȵ�ϡ������ǡ����ȫ��Ӧ����ʱ��Һ��pH��7��Ȼ���ټ�����������������Һ�õ���ɫ����57.4g���Է������㣺
��1��50g�����Һ��̼���Ƶ�����Ϊ_____g��
��2��50g�����Һ���Ȼ��Ƶ����������Ƕ��٣�_____��д��������̣���������ȷ��0.1%��
����Ŀ��Ϊ�ⶨCuCl2��FeCl2��ɵĻ����Һ��FeCl2����������,��������ʵ��:
��ȡ200g�����Һ����������AgNO3��Һ,�����ˡ�ϴ�ӡ��������,�õ�143.5gAgCl���壻����ȡԭ�����Һ��200g�뺬�����ʵķ���м��Ӧ(���ʲ�����ˮ,Ҳ�����뷴Ӧ),����������ʵ��,��ʵ���������±���
ʵ����� | һ | �� | �� | �� | �� |
�����Һ����/g | 200 | 200 | 200 | 200 | 200 |
�����/g | 6 | 9 | 12 | 15 | 18 |
����ͭ������/g | 6.4 | 9.6 | m | 16 | 16 |
���������:
(1)���е�����ʵ���mֵΪ_______��
(2)��_____��ʵ��ǡ����ȫ��Ӧ��
(3)��м��������������Ϊ����___________?(��������ȷ��0.1%)
(4)ԭ�����Һ��FeCl2����������Ϊ����______________?(��������ȷ��0.1%)
����Ŀ��ij�������Ӫ���ɷֱ����(����̼ˮ��������Ҫָ���۵�)��
Ӫ���ɷֱ� |
��Ŀÿ100�� |
���� 1966ǧ�� ������ 7.5�� ֬�� 21.8�� ̼ˮ������ 60.7�� �� 2300���� |
(1)������������ָ_____(����ĸ���)��
A ����B ���� C Ԫ��D ����
(2)�÷������к���Ӫ������_____�֡�
(3)��������ʹ�õ�ʳ�ο����Ǽӵ��Σ�������ȱ����ܻ��еļ�����_____(������״���״�����������������)��
(4)������ͨ�����þ��������ϴ���װ�������������������ɫ��Ⱦ������������_____���ϡ�
(5)�й�������ʳָ�Ͻ���ÿ��ʳ��ʳ��ʯ����6�ˣ�����С��ij�����100�˸÷����棬�൱�ڳ���ʳ��_____�ˡ�(����С�����һλ)