题目内容
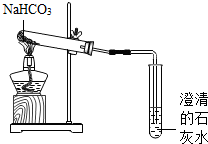 NaHCO3是一种重要的盐,设计实验探究其性质.
NaHCO3是一种重要的盐,设计实验探究其性质.(1)向NaHCO3溶液中,滴入酚酞溶液,振荡,溶液变成红色,说明其溶液呈
(2)按如图装置实验,充分加热后,试管中留下的白色固体只有Na2CO3,由此可知,要除Na2CO3中混有的NaHCO3可选用的方法是
考点:盐的化学性质
专题:常见的盐 化学肥料
分析:(1)考虑酸碱指示剂的变色规律;
(2)根据题目中的信息“充分加热后,试管中留下的白色固体只有Na2CO3”,进行分析.
(2)根据题目中的信息“充分加热后,试管中留下的白色固体只有Na2CO3”,进行分析.
解答:解:
(1)根据“蕊酸红,蕊碱蓝,酚酸无,酚碱红”,则“向NaHCO3溶液中,滴入酚酞溶液,振荡,溶液变成红色”,说明碳酸氢钠溶液呈碱性.
(2)因为碳酸氢钠“充分加热后,试管中留下的白色固体只有Na2CO3”,故要除Na2CO3中混有的NaHCO3可选用的方法是加热,因为充分加热后,碳酸氢钠分解生成白色固体Na2CO3.
故答案为:
(1)碱性;(2)加热
(1)根据“蕊酸红,蕊碱蓝,酚酸无,酚碱红”,则“向NaHCO3溶液中,滴入酚酞溶液,振荡,溶液变成红色”,说明碳酸氢钠溶液呈碱性.
(2)因为碳酸氢钠“充分加热后,试管中留下的白色固体只有Na2CO3”,故要除Na2CO3中混有的NaHCO3可选用的方法是加热,因为充分加热后,碳酸氢钠分解生成白色固体Na2CO3.
故答案为:
(1)碱性;(2)加热
点评:本题主要考查了酸碱指示剂的变色规律和碳酸氢钠受热易分解的化学性质.

练习册系列答案
相关题目
下列有关K2CO3的说法中,错误的是( )
| A、可用作钾肥 | ||
| B、其中碳、氧元素的质量比为1:4 | ||
| C、K2CO3中碳元素的化合价为+4 | ||
D、其中钾元素的质量分数为
|