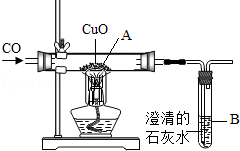
题目内容
初中化学课上,同学们利用下列实验探究碱的化学性质: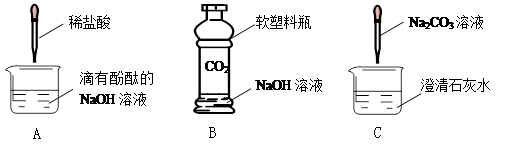
1)A实验中观察到的现象为 ,原因是(用化学方程式表示) 。
2)B实验中反应的化学方程式为 。
3)C实验中观察到的现象是 。
4)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】 废液中含有什么物质?
【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有 。
老师问:废液中还可能有什么物质?引发同学们热烈讨论,下面是大家的发言:
| 学生甲 | 可能有Ca(OH)2、NaOH | 学生丙 | 可能有Ca(OH)2、CaCl2 |
| 学生乙 | 可能有NaOH、Na2CO3 | 学生丁 | 可能有Na2CO3 |
| 学生戊 | 可能有NaOH | …… | ………… |
【实验验证】 同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。
【结论】上述滤液中,还含有 ,没有 。
1)溶液红色逐渐褪去, HCl + NaOH = NaCl + H2O
2)CO2 + 2NaOH = Na2CO3 + H2O
3)有白色浑浊生成(或白色沉淀生成)
4)【猜想】NaCl
【结论】Na2CO3 , CaCl2、Ca(OH)2、NaOH
解析试题分析:1)氢氧化钠溶液呈碱性,可使酚酞变红。当加入稀盐酸后,二者发生中和反应。随着稀盐酸的加入,溶液的碱性会逐渐减弱至中性或酸性。观察的现象是:溶液红色会逐渐褪去。反应的化学方程式为:HCl + NaOH = NaCl + H2O
2)B中的二氧化碳会与氢氧化钠反应生成碳酸盐和水,反应的化学方程式为:CO2 + 2NaOH = Na2CO3 + H2O
3)石灰水是氢氧化钙的水溶液,会与碳酸钠反应生成白色的难溶于水的碳酸钙和水。所以反应的现象为:有白色沉淀生成。
4)【猜想】A中会生成氯化钠。且氯化钠不与后面的物质反应,因此一定存在。B中会生成碳酸钠。实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。说明C中的氢氧化钙有剩余,并与B中生成的碳酸钠反应生成碳酸钙沉淀而浑浊。由于碳酸钠参与了反应,所以它不一定存在,而是可能存在。显红色说明溶液呈碱性。在上述实验中呈碱性的有氢氧化钠、碳酸钠或氢氧化钙。无法确定哪一种。如A中盐酸有剩余,则可能存在还有氯化钙。因此一定存在的是氯化钠。
【结论】取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。说明溶液中存在的碱性物质能与氯化钡反应,所以应为碳酸钠。由氯化钙、氢氧化钙一定不存在。最终溶液为无色,可确定氢氧化钠也不存在。
考点:科学探究、酸碱盐间的反应、过量推断

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石与稀盐酸制取),对反应后反应器中剩余溶液的溶质成分产生了兴趣。他们继续进行了如下实验探究。
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙,但其中是否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有
H+),说明含有氯化氢。
【查阅资料】碳酸钙不溶于水,氯化钙溶液不显酸性。
【实验过程】
将剩余溶液倒入烧杯中,微热后冷却至室温。
| | 实验操作 | 实验现象 | 实验结论 |
| 甲同学 | 取烧杯中溶液少许于试管中,向其中滴加 | 现象:溶液变为红色 | 溶液显酸性(含有H+),溶质中有氯化氢 |
| 乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象: 反应的化学方程式是: | |
| 丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量石灰石 | 现象: |
【拓展提高】若要从剩余溶液中得到尽可能多的纯净的氯化钙固体,同学们认为可以向剩余溶液中加入稍过量的 (填化学式),经 ,蒸发等操作后即可完成。
小芳同学从超市购买了一瓶维生素C泡腾片。下图是标签上的部分内容。
| 维生素C泡腾片 功能:补充人体维生素C,增强机体抵抗力 主要成分:维生素C 辅料成分:碳酸氢钠、氯化钠、酒石酸晶体、蔗糖、糖精钠、阿朴胡萝卜醛、橘味香精、橙味香精、维生素B 贮藏:低温、避光、防潮 |
小芳同学根据使用说明将维生素C泡腾片放入一杯水中,发现维生素C泡腾片逐渐溶解,产生大量气泡,片刻后变为一杯鲜甜的橙味饮品。小芳同学感到很好奇,产生的气泡是什么呢?
请你参与小芳同学的探究:
【提出问题】维生素C泡腾片放入水中,产生的气泡是什么呢?
【我的猜想】气体成分是________,理由是_________________________。
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 |
| 将一片维生素C泡腾片放入水中,将产生的气体通入__ __________________ | | |
根据维生素C泡腾片储存条件,请说明保存时要低温和防潮的原因是:
①______________________________________________________;
②______________________________________________________。
某同学欲探究市售 “双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分。
【查阅资料】
(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分构成。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3) 和水合硅酸(SiO2·nH2O)等
(3)牙膏和牙粉中除了碳酸钙以外,其它物质均不与稀盐酸反应产生气体。
【实验一】探究“两种牙膏和牙粉中是否都含有碳酸钙?
| 步骤 | 实验操作 | 实验现象 |
| ① |  如图所示,取三只试管分别加入适量待测样品,再分别加入适量R 溶液。R 溶液是 。 | A试管中无明显变化, B和C试管中有无色气体生成。 |
| ② | 将B和C试管中生成的无色气体通入澄清石灰水。 | 现象Ⅱ: 。 |
实验结论: 。
【实验二】比较样品中碳酸钙的含量
| 步骤 | 实验操作 | 实验现象 |
| ① | 组装两套如图装置进行实验。分别取 (操作Ⅰ),放于锥形瓶中。并在分液漏斗中分别加入等质量的R 溶液。  | |
| ② | 打开分液漏斗注入一定量R 溶液,然后关闭活塞。 | 有气泡产生。 |
| ③ | 待②反应结束后,再打开分液漏斗,注入一定量R 溶液,然后关闭活塞。 | 无明显现象 |
| ④ | 称量反应后装置及药品的总质量并加以比较 | 加入“双钙防蛀”牙膏的装置及药品的总质量大于加入牙粉的装置及药品的总质量 |
实验结论:_____________________________________________________
步骤③的作用是: 。
【反思】
(1)若不改动原有装置和基本步骤,要测定牙粉中碳酸钙的质量分数,还应测定的数据有:_______________________________________________________________
(2)小明认为该实验前不需要测定装置的气密性,请你说明其原因 。