题目内容
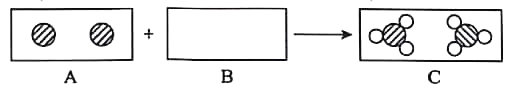
【题目】已知A﹣H均为初中化学常见的物质,其中A、C是组成元素相同的气体,且C能产生温室效应;B是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
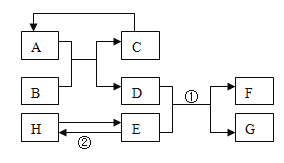
(1)C的化学式:______.
(2)写出一个符合反应②的化学方程式______.
(3)我国工业制硫酸的第一步反应是硫铁矿(主要成分为FeS2)即FeS2与氧气在高温条件下反应生成B和二氧化硫,写出该反应的化学方程式______.
【答案】CO2 ![]()
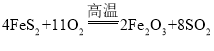
【解析】
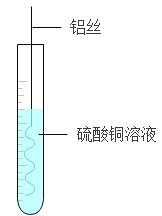
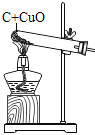
C能产生温室效应,可推出C为二氧化碳,A、C是组成元素相同的气体,可推出A为一氧化碳,B是赤铁矿的主要成分,因此B是三氧化二铁,三氧化二铁能与一氧化碳在高温的条件下反应生成铁和二氧化碳,可推出D为铁,F为紫红色金属,可推出F为铜,铁能与E反应生成铜,铁能与可溶性铜盐(如硫酸铜)反应生成铜和亚铁盐溶液,可推出E为铜盐溶液,如硫酸铜,则G为硫酸亚铁,H是蓝色沉淀,可推出H为氢氧化铜。
(1)由上述分析可知C是二氧化碳,化学式是CO2;
(2)由上述分析可知D为铁,E为铜盐溶液,铜盐溶液与碱反应可制取氢氧化铜沉淀,如硫酸铜和氢氧化钠反应生成氢氧化铜和硫酸钠,该反应的化学方程式为:![]() ;
;
(3)B为三氧化二铁,硫铁矿主要含FeS2,在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,反应的化学方程式为: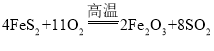 。
。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案【题目】如图所示装置进行实验(图中铁架台等仪器均已略去)。在I中加入试剂后,塞紧橡皮塞,立即打开止水夹,II中有气泡冒出;一段时间后关闭止水夹,II中液面上升,溶液由无色变为浑浊。符合以上实验现象的I和II中应加入的试剂是
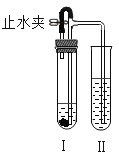
A | B | C | D | |
I | 大理石、稀盐酸 | 紫铜、稀硫酸 | 锌粒、稀盐酸 | 纯碱、稀硫酸 |
II | 硝酸钾溶液 | 氢氧化钡溶液 | 硝酸银溶液 | 氯化钠溶液 |
A.AB.BC.CD.D
【题目】为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取40 g石灰石样品分为4等份进行实验。所得数据如下表所示:
实验编号 | ① | ② | ③ | ④ |
稀盐酸的质量/g | 25 | 50 | m | 150 |
剩余固体的质量/g | 7.5 | 5 | 2 | 2 |
(1)石灰石的纯度是__________。
(2)计算所用稀盐酸的溶质质量分数_______。(写出计算过程)
(3)表中m的值________(填“大于”“小于”或“等于”)100 g。