题目内容
【题目】水是宝贵的自然资源。
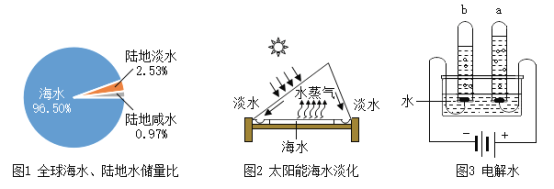
(1)图1中的海水属于_____(填“纯净物”或“混合物”)。除去海水中难溶性杂质的操作是_____。
(2)海水淡化可缓解淡水资源匮乏的问题。图2中水发生的是_____(填“物理”或“化学”)变化,这个过程中水分子的_____发生了改变。
(3)图3试管a内气体的检验方法是_____,水电解过程中不发生变化的微粒是_____。
(![]() 表示一个水分子,填字母序号)
表示一个水分子,填字母序号)
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]() E.
E. ![]()
(4)水是常见的溶剂。甲、乙两种固体的溶解度曲线如图一所示:
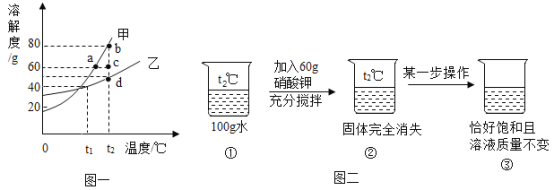
Ⅰ.t1℃时, 溶解度大小关系为:甲_____乙(填“>”、“<”或“=”);
Ⅱ.t2℃时,100g水中最多溶解甲物质_____g;
Ⅲ.由图二推测硝酸钾是图一中的_____(填“甲”或“乙”)物质;
Ⅳ.图二操作II前后的溶液状态变化过程可以在图一中表示为_____(填序号)。
A b点→a点
B c点→a点
C c点→b点
D c点→d点
【答案】混合物 过滤 物理 间隙 带火星的木条复燃则为氧气 D、E > 80 甲 B、C
【解析】
(1)海水由水和溶于水的多种物质组成,属于混合物。除去海水中难溶性杂质的操作是过滤;
(2)图2所示是水的蒸馏,过程中水只发生了状态的变化,没有新的物质生成,是物理变化,这个过程中水分子的间隙和排列方式发生了改变,分子的种类不变;
(3)电解水时,正极产生氧气,负极产生氢气,氢气是氧气体积的2倍,图3试管a内气体为氧气,检验方法是带火星的木条复燃则为氧气,原子是化学变化中最小的微粒,水电解过程中不发生变化的微粒是氢原子和氧原子(D、E);
(4)Ⅰ.由图可知,t1℃时, 溶解度大小关系为:甲>乙;
Ⅱ. 由图可知,t2℃时,甲的溶解度为80g,即:t2℃时,100g水中最多溶解甲物质80 g;
Ⅲ. 由图可知,t2℃时甲的溶解度大于60g,乙的溶解度小于60g,所以由60g硝酸钾能完全溶解,可知图二中硝酸钾是图一中的甲物质;
Ⅳ.图二所示操作II中溶液状态变化过程是由不饱和溶液转化成饱和溶液,则:
A、b点→a点,表示的是将t2℃时硝酸钾的饱和溶液降温至a点,得该温度下的饱和溶液,但实际上,操作II前溶液是不饱和溶液,选项错误;
B、“c点”是t2℃时,向100g水中放入60g硝酸钾所得的不饱和溶液,“→a点”,是降温得到a点的溶液, a点时,硝酸钾的溶解度为60g,溶液刚好达到饱和,选项正确;
C、c点→b点,是指在不改变温度的条件下,增加溶质,变成饱和溶液,选项正确;
D、c点→d点都是硝酸钾在t2℃时的不饱和溶液,选项错误。
故选BC。

 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
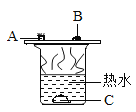
开心蛙状元作业系列答案【题目】如图所示,将一定量的液体 X 滴入到烧瓶中,若小气球先鼓起,一段时间后又变瘪(液体 X的体积忽略不计),则液体 X 和固体 Y 是( )
选项 | 液体X | 固体Y |
A | 水 | 氧氧化钠 |
B | 水 | 碳酸铵 |
C | 过氧化氢溶液 | 二氧化锰 |
D | 稀盐酸 | 碳酸钠 |
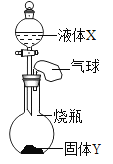
A.AB.BC.CD.D
【题目】下表列出一些常见燃料的化学式及完全燃烧放出的热量。
燃料 | 一氧化碳 | 氢气 | 甲烷 | 酒精 |
化学式 | CO | H2 | CH4 | C2H5OH |
热量(×106J/Kg) | 9.2 | 141.6 | 55.6 | 29.7 |
(1)甲烷属于_____(填“有机化合物”或“无机化合物”)。
(2)二氧化碳是温室气体之一。使用上述中燃料的_____能有效缓解温室效应。
(3)写出酒精燃烧的化学方程式_____。
(4)酒精是易燃物,要在低温阴凉处储存,此外还要注意_____。
(5)请结合上表,写出-条家用燃料从管道煤气(主要成分CO)发展到天然气(主要成分CH4)的优点_____。
【题目】校化学兴趣小组欲对市售的某些牙背、牙粉进行探究。以下是A牙膏、B牙膏、C牙粉商标上摩擦剂的主要成分。
A牙膏 | B牙膏 | C牙粉 |
氢氧化铝、碳酸钙 | 碳酸钙 | 碳酸钙 |
查阅资料:氢氧化铝固体既能与酸反应生成盐和水,也能和碱反应生成盐和水(牙膏和牙粉中除了摩擦剂以外,其它物质均不与酸、碱反应)。
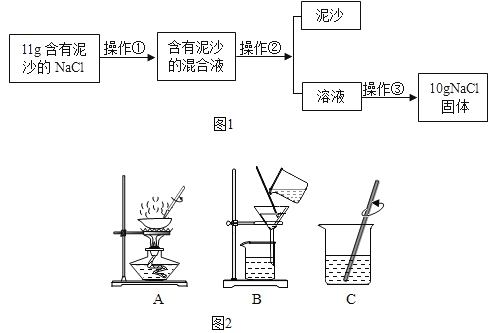
实验一:验证 A牙膏中含有氢氧化铝、碳酸钙,实验设计如下:
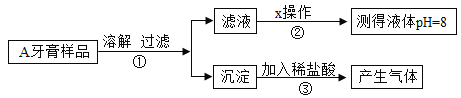
(1)步骤②中x的具体操作过程是_____。
(2)从步骤③的探究结果可知A牙膏中一定含有碳酸钙摩擦剂,原因用化学方程式表示为_____。
(3)为进一步证明氢氧化铝存在,向过滤所得沉淀中加入_____,当观察到_____,可以证明氢氧化铝存在。
实验二:比较B 牙膏和C牙粉中碳酸钙含量的多少,实验设计如下:
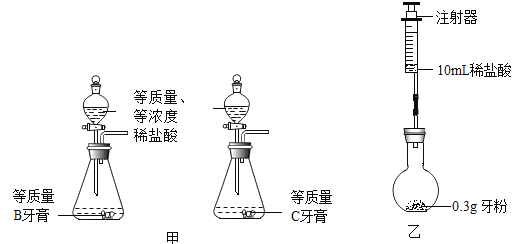
步骤 | 实验操作 | 实验现象 |
① | 用同一套装置先后进行两次实验,装入药品如图甲 | |
② | 打开分液漏斗活塞注入一定量稀盐酸,然后关闭活塞 | 有气泡产生 |
③ | 待②反应结束后,再打开分液漏斗活塞,注入一定量稀盐酸,然后关闭活塞 | 无明显现象 |
④ | 称量反应后装置及药品的总质量并比较 | 加入B牙膏的装置及药品的总质量大于加入C牙粉的装置及药品的总质量 |
(4)实验结论为_____。
(5)步骤③的作用是_____。
(6)有同学认为该实验前可以不检查装置的气密性,你是否认同?并说明原因_____。
实验三:测定C牙粉中碳酸钙的含量
(7)方案一:若不改动实验二的装置和基本步骤,要测定牙粉中碳酸钙的质量分数,还应测定的数据有_____。
(8)方案二:取C牙粉0.3g放入图乙装置,再将注射器中10mL稀盐酸迅速压入烧瓶中。实验记录如下:
时间/min | 1 | 3 | 5 | 7 | 8 | 9 | 10 |
注射器读数/mL | 40.0 | 59.0 | 60.0 | 60.4 | 60.5 | 60.5 | 60.5 |
综合分析以上实验过程和数据,最终生成气体的体积是_____mL。根据气体体积计算其质量,进而计算C牙粉中碳酸钙的含量。