题目内容
【题目】明确宏观现象的微观本质是学习化学的重要思想方法:
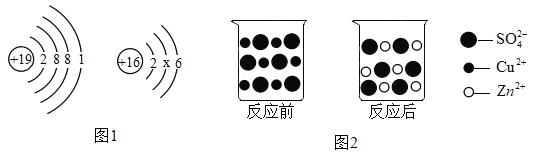
(1)如图1是钾原子和硫原子的结构示意图,请回答:
①x的数值是___________________________。
②钾原子在化学反应中易________________电子(填“得到”或“失去”)。
③钾元素和硫元素形成的化合物硫化钾的化学式是________________。
(2)图2是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。锌与硫酸铜溶液发生反应过程中变化的微观粒子是________________,该反应的化学方程式为________________。
【答案】8 失去 K2S 锌原子和铜离子 ![]()
【解析】
(1)①原子的核内质子数=原子的核外电子数,故16=2+x+6,x=8;
②钾原子的最外层电子数为1,小于4,在化学反应中易失去电子;
③钾原子的最外层电子数为1,在化学反应中容易失去1个电子,从而带上1个单位的正电荷,硫原子的最外层电子数为6,在化学反应中,容易得到电子,从而带上2个单位的负电荷,故钾元素和硫元素形成的化合物硫化钾的化学式是:K2S;
(2)由图可知,锌与硫酸铜溶液发生反应过程中变化的微观粒子是:锌原子与铜离子;
锌与硫酸铜反应生成了硫酸锌和铜,该反应的化学方程式为:![]() 。
。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】实验是学习化学的重要方法,下列实验设计不能实现相应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
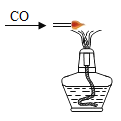
A | 除去CO2中少量的CO |
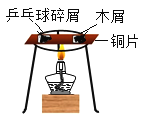
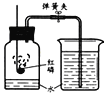
| B | 探究不同物质的着火点不同 |
|
C | 探究CO2的化学性质 |
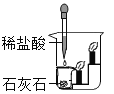
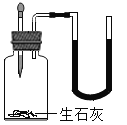
| D | 探究生石灰与水反应是否放热 |
|
A.AB.BC.CD.D
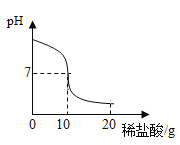
【题目】将20.0g稀盐酸逐滴加入到10.0g溶质质量分数为40%的氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的pH变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)
反应时间(s) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶液温度(℃) | 20.5 | 20.6 | 20.7 | 20.8 | 20.9 | 20.8 | 20.7 |
(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是_____℃
(2)计算稀盐酸中溶质的质量分数_________(精确到0.1%)