题目内容
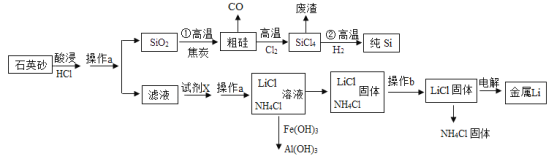
【题目】首届中国国际钢铁流通博览会以“困境与出路”为主题,将发展网上钢贸交易平台,钢材条形码有价格、产地等信息。则:
(1)生铁和钢是_____不同的两种铁合金,都属于_____(填“纯净物”或“混合物”)。
(2)为了探究铁与锰的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中(反应中的Mn元素显+2价)。请回答:
金属 | 铁 | 锰 |
分别与盐酸反应的现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
得出结论 | 得出活动性:铁_____(填“>”“<”)锰 | |
(3)写出锰与稀盐酸发生反应的化学方程式为____________,该反应的基本类型为____。
【答案】含碳量 混合物 < Mn+2HCl=MnCl2+H2↑ 置换反应。
【解析】
(1)生铁和钢都是铁和碳的合金,都是铁和碳的混合物,只是含碳量不同,生铁的含碳量为![]() ,钢的含碳量为
,钢的含碳量为![]() 。
。
故答案为:含碳量;混合物。
(2)在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质质量分数的足量稀盐酸中,控制好其它变量相同,唯一不同的变量只是金属的种类铁和锰,现象是锰比铁与盐酸反应放出的气泡速率快,说明锰的金属活动性比铁强。
故答案为:<。
(3)锰与盐酸反应产生气泡,反应中Mn元素显+2价,故生成的氯化锰的化学式为MnCl2,反应的方程式为:Mn+2HCl=MnCl2+H2↑。该反应符合一种单质Mn与一种化合物HCl反应生成另一种单质H2与另一种化合物MnCl2,即为置换反应。
故答案为:Mn+2HCl=MnCl2+H2↑;置换反应。

 单元期中期末卷系列答案
单元期中期末卷系列答案【题目】现有一家庭食用纯碱样品,其中含杂质氯化钠(不含其他杂质),为了测定样品中杂质氯化钠的质量分数,李明同学进行了三次实验。实验数据如下表:
编号 | 第1次 | 第2次 | 第3次 |
所取固体样品的质量g | 15 | 12 | 12 |
加入氯化钙溶液的质量/g | 100 | 100 | 150 |
反应后生成沉淀的质量/g | 10 | 10 | 10 |
完成下列计算(计算结果精确到0.1%):
(1)第_______次实验是恰好完全反应。
(2)加入氯化钙溶液的溶质质量分数。______
(3)样品中氯化钠的质量分数。_______
【题目】彩漂洗衣液能够去渍、除菌,白色和彩色织物均可使用。彩漂洗衣液中含有过氧化氢。实验小组对过氧化氢的某些性质进行探究。

[使用说明]每2L水加入1瓶盖本品,与洗衣粉混合浸泡效果更佳;遇顽固污渍,可适当提高水温或延长浸泡时间。注意:使用彩漂液清洗彩色衣服时水温不宜超过50°C!
[进行实验]探究过氧化氢溶液的漂白性。
实验1:室温下用10%的过氧化氢溶液浸泡一块红色布条,浸泡时间与布条颜色变化如下表。
浸泡时间 | 20分钟 | 40分钟 | 60分钟 |
布条颜色的变化 | 无明显变化 | 颜色稍变浅 | 颜色明显变浅 |
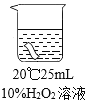
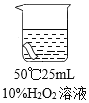
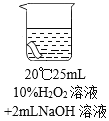
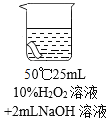
实验2:将红色布条分别浸泡在4种溶液中,20 分钟后现象如下表。
编号 | ① | ② | ③ | ④ |
实验 |
|
|
|
|
布条颜色的变化 | 无明显变化 | 颜色稍变浅 | 颜色稍变浅 | 颜色明显变浅 |
[解释与结论]
(1)实验1的目的是探究_____________对H2O2溶液漂白效果的影响。
(2)实验2中,欲得出“其他条件相同时,升高温度可使过氧化氢溶液的漂白性增强”的结论,需要对比实验______________
(3) 实验2中,通过对比②④,得出的结论是__________。
(4)根据上述实验,推测“使用彩漂液清洗彩色衣服时水温不宜超过50°C”的原因是________。
[注意:若答对第(5) (6) 小题奖励4分,化学试卷总分不超过60分。]
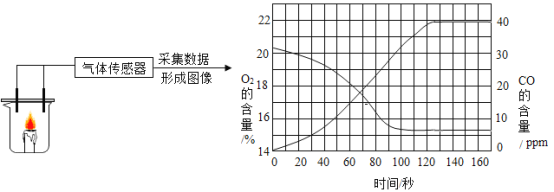
实验小组查得知,FeCl2 溶液对过氧化氢溶液分解有催化效果,在老师的指导下设计以下实验:向两支试管中分别加入等质量不同浓度(5%和2%)的H2O2溶液,再同时用注射器匀速注入等质量、等浓度的FeCl3溶液,分别用气压传感器测定(装置气密性良好)两试管中气体压力的变化曲线如图所示:
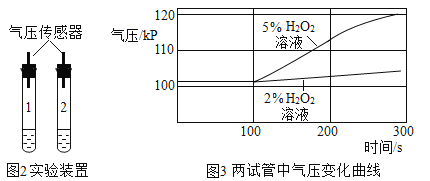
(5)图2中0-100秒管内气压几乎没有变化的可能原因是________;请你再从图2曲线中找FeCl3溶液对H2O2溶液分解影响的一条规律性结论:_______。
(6)请设计实验证明是FeCl3溶液中的Fe3+ 对过氧化氢溶液分解有催化效果:_______(包括实验步骤和预期现象)