题目内容
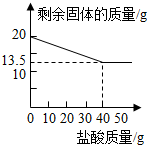 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称量,5次稀盐酸用量和剩余固体质量记录如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称量,5次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| 1 | 10 | 18.375 |
| 2 | 10 | 16.750 |
| 3 | 10 | 15.125 |
| 4 | 10 | 13.500 |
| 5 | 10 | 13.500 |
(2)计算稀盐酸中溶质的质量分数;
(3)当合金中的锌与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为多少?
分析:(1)剩余固体是铜,根据铜的质量和假黄金的质量可以计算出合金中锌的质量分数.
(2)由曲线图看出加入40g盐酸后恰好完全反应反应,由锌和完全反应时盐酸的质量根据锌与盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数和生成氯化锌、氢气的质量.
(3)由氯化锌、合金、铜、氢气和恰好完全反应时盐酸的质量,可以计算出此时所得溶液中溶质的质量分数.
(2)由曲线图看出加入40g盐酸后恰好完全反应反应,由锌和完全反应时盐酸的质量根据锌与盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数和生成氯化锌、氢气的质量.
(3)由氯化锌、合金、铜、氢气和恰好完全反应时盐酸的质量,可以计算出此时所得溶液中溶质的质量分数.
解答:解:(1)合金中锌的质量分数为
×100%=32.5%
(2)设稀盐酸中溶质的质量分数为x,生成氯化锌的质量为y,生成氢气的质量为z.
Zn+2HCl=ZnCl2+H2↑
65 73 136 2
20g-13.5g 40g?x y z
=
=
=
x=18.25%,y=13.6g,z=0.2g
(3)恰好完全反应时,所得溶液中溶质的质量分数为
×100%≈29.4%
答:(1)合金中锌的质量分数为32.5%.
(2)稀盐酸中溶质的质量分数为18.25%.
(3)恰好完全反应时所得溶液的质量分数为29.4%.
| 20g-13.5g |
| 20g |
(2)设稀盐酸中溶质的质量分数为x,生成氯化锌的质量为y,生成氢气的质量为z.
Zn+2HCl=ZnCl2+H2↑
65 73 136 2
20g-13.5g 40g?x y z
| 65 |
| 20g-13.5g |
| 73 |
| 40g?x |
| 136 |
| y |
| 2 |
| z |
x=18.25%,y=13.6g,z=0.2g
(3)恰好完全反应时,所得溶液中溶质的质量分数为
| 13.6g |
| 20g+40g-13.5g-0.2g |
答:(1)合金中锌的质量分数为32.5%.
(2)稀盐酸中溶质的质量分数为18.25%.
(3)恰好完全反应时所得溶液的质量分数为29.4%.
点评:本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
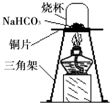 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.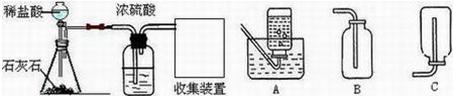
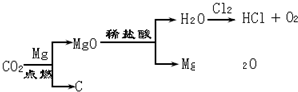
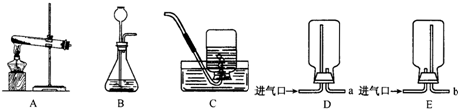
 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.