题目内容
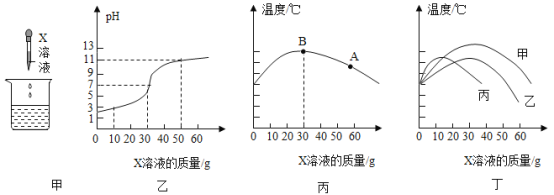
【题目】某实验探究小组用氢氧化钠溶液和稀硫酸进行中和反应的实验探究(如图甲)
(1)写出该化学反应方程式_____。
(2)兴趣小组用 pH 探测仪测得烧杯内溶液 pH 的变化(如图乙),则实验中烧杯内所加入的溶液是_____。
(3)兴趣小组同学用温度传感器测得烧杯内温度变化图像(如图丙) (实验过程中保温良好,热量散失忽略不计),该图说明该中和反应____________(吸热或者放热),为确定A 点对应的溶液中所含微粒,该同学设计如下实验。
操作 | 现象 | 结论 |
从烧杯内取少量溶液,向溶液中加入硫酸铜溶液 | ____________ | A 点对应的溶液中所含微粒有:_____ |
[实验反思]
实验小组其他同学也绘制了实验过程中温度变化图像(如图丁)(实验过程中保温良好,热量散失忽略不计)。实验中各同学所得温度变化图像不同的原因可能是________________。
【答案】2NaOH+H2SO4=Na2SO4+2H2O 稀硫酸 放热 有蓝色沉淀产生 Na+、OH—、SO42—、H2O 所用氢氧化钠溶液以及稀硫酸的浓度不同 或所用氢氧化钠溶液以及稀硫酸的质量不同等
【解析】
(1)氢氧化钠和硫酸反应生成硫酸钠和水的化学反应方程式为:
2NaOH+H2SO4=Na2SO4+2H2O 。
(2)图像中溶液的 pH 值是从小于 7 逐渐的增大到大于 7,则实验中烧杯内所加入的溶液是稀硫酸,先酸性,pH小于7。
(3)由温度传感器测得烧杯内温度变化图像可知,随着反应的进行,温度升高,反应结束, 温度降低,该图说明该中和反应放热。
B 点温度达到最大值,说明氢氧化钠和硫酸恰好完全反应,A 点表示氢氧化钠是过量的, 则A 点对应的溶液中溶质为硫酸钠、氢氧化钠。所以,从烧杯内取少量溶液,向溶液中加入硫酸铜溶液与氢氧化钠反应产生氢氧化铜蓝色沉淀和硫酸钠溶液,A 点对应的溶液中所含微粒有:Na+、OH—、SO42—、H2O;
[实验反思]
实验中各同学所得温度变化图像不同的原因:可能是所用氢氧化钠溶液以及稀硫酸的浓度不同或所用氢氧化钠溶液以及稀硫酸的质量不同等。