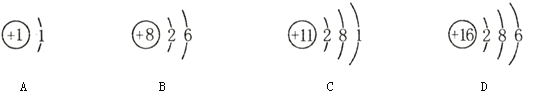题目内容
【题目】黄铁矿矿石的主要成分为二硫化亚铁(FeS2),取一块质量为30克的黄铁矿矿石样品在氧气中完全灼烧后得到10克氧化铁(其中的铁全来自二硫化亚铁)同时生成二氧化硫。
(1)二硫化亚铁中硫元素的化合价为
(2)计算黄铁矿矿石样品中二硫化亚铁的质量分数。
【答案】(1)--1; (2)50%
【解析】
试题分析:(1)根据化学式中元素的正负化合价的代数和为零计算,在二硫化亚铁(FeS2)中,铁元素的化合价为+2价,设硫元素的化合价为x;2x+2=0;得到x= —1;
(2)设黄铁矿矿石样品中二硫化亚铁的质量为x
4FeS2+11O2![]() 2 Fe2O3+8SO2
2 Fe2O3+8SO2
480 320
X 10g
480/x=320/10g
X=15g
黄铁矿矿石样品中二硫化亚铁的质量分数为:15g/30g×100%=50%
答; 二硫化亚铁中硫元素的化合价为—1价,黄铁矿矿石样品中二硫化亚铁的质量分数50%

 阅读快车系列答案
阅读快车系列答案【题目】
[查阅资料]有些水果、蔬菜对过氧化氢的分解有催化作用。
[实验探究1]探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
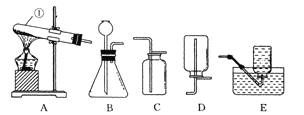
各量取6ml的过氧化氢溶液,分别倒入1、2、3号三志试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管口内,观察现象并记录如下:
试管编号 | 1 | 2 | 3 | |
材料名称 | 无 | 苹果 | 土豆 | |
实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
产生气泡 | 很少 | 比1中多 | 较多 | |
复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
实验结论 | ||||
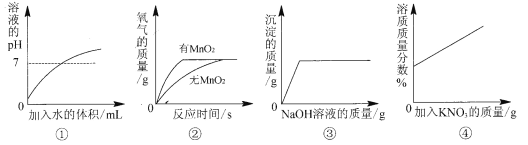
[实验探究2]探究浓度对过氧化氢分解速率的影响:
取10ml30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100ml氧气所用的时间,(其它实验条件均相同)记录如下:
实验编号 | 1 | 2 | 3 |
过氧化氢溶液浓度 | 5% | 15% | 30% |
所用时间(秒) | 205 | 25 | 3 |
实验结论 | |||
[实验条件3]用上述收集的仪器与不同位置进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,该反应的化学方程式为: 。