题目内容
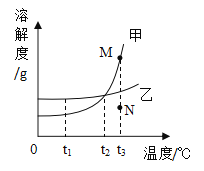
【题目】如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是
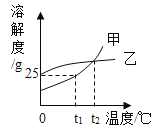
A.t1℃时,25g甲充分溶解于100g水中,可得甲的饱和溶液125g
B.t2℃时,甲、乙的溶液的溶质质量分数相等
C.若甲中含有少量乙,可用降温结晶的方法提纯甲
D.将t2℃时的甲的饱和溶液降温到t1℃,可析出晶体
【答案】B
【解析】
A、t1℃时,甲的溶解度为25g,根据溶解度概念可知,25g甲充分溶解于100g水中,可得甲的饱和溶液125g,故A正确;
B、t2℃时,甲和乙的溶解度相等,一定温度下饱和溶液的溶质质量分数=![]() ,故甲、乙饱和溶液的溶质质量分数相等,但题中没有确定溶液是否饱和,无法确定溶质质量分数大小关系,故B错误;
,故甲、乙饱和溶液的溶质质量分数相等,但题中没有确定溶液是否饱和,无法确定溶质质量分数大小关系,故B错误;
C、甲的溶解度受温度的影响较大,故甲中含有少量乙,可用降温结晶的方法提纯甲,故C正确;
D、甲的溶解度随温度的升高而增大,故将甲的饱和溶液从t2℃时降温到t1℃,溶解度变小,可析出晶体,故D正确。故选B。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
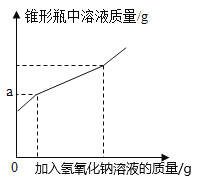
【题目】现有盐酸和铁锈反应后的溶液,为测定溶液中氯化铁的含量,某化学活动小组称取样品溶液50g放入锥形瓶中,再向锥形瓶中滴加氢氧化钠溶液,反应过程中产生沉淀质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
加入氢氧化钠溶液的质量/g | 70 | 90 | 120 | 140 |
产生沉淀的质量/g | 2.14 | 3.21 | 4.28 | m |
(1)表中m的值是 ;
(2)50克样品中氯化铁的质量分数是 ;
(3)求该实验中所用氢氧化钠溶液的溶质质量分数。(写出计算过程)
(4)如图图象中a的数值是 。