题目内容
【题目】为了测定稀盐酸的溶质质量分数,实验小组同学决定用一根在家中杂物堆存放已久的小铁钉,与稀盐酸反应进行数字收集。实验过程有关内容以图像的形式记录如下图,其中产生氢气的化学方程式为:Fe + 2HCl=FeCl2+ H2↑ 。
试回答以下问题:
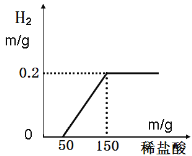
①铁钉与稀盐酸完全反应后产生氢气的质量为_______克。产生这份氢气共用去盐酸的质量为________克。
②计算实验所用盐酸溶质质量分数__________。
【答案】 0.2 100 7.3%
【解析】根据图像可知产生氢气的质量是0.2g,所用的盐酸的质量为150g-50g=100g。
解:设实验所用盐酸的质量分数为x
Fe + 2HCl=FeCl2+ H2↑
73 2
100g×x 0.2g
![]()
![]()
答:实验所用盐酸溶质质量分数为7.3%。

练习册系列答案
相关题目
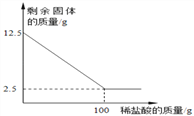
【题目】一些骗子常用黄铜冒充黄金骗取钱财,某同学通过查阅资料得知黄铜是锌和铜的合金,他取一定量的某黄铜样品放入烧杯中,再向其中分4次加入等质量的同一稀硫酸,每次均充分反应。实验过程中有关物质的用量及质量测定记录如下表:
实验次数 | 1 | 2 | 3 | 4 |
稀硫酸的用量/g | 20 | 20 | 20 | 20 |
剩余固体的质量 | 10 | 8.7 | 7.4 | 7.2 |
分析表中数据,完成下列问题:
(1)所取黄铜样品的质量为___________ g;
(2)第4次实验结束后溶液的pH __________7(填“>”、“=”或“<”);
(3)所用稀硫酸中溶质的质量分数为________________?(要求有解答过程)