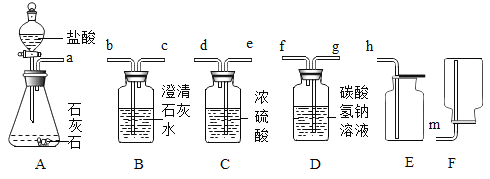
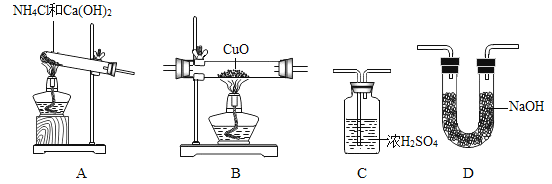
题目内容
【题目】镁和铝都是很重要的金属材料。
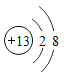
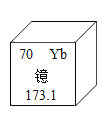
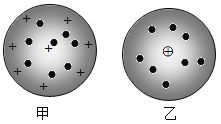
(1)如图是铝的微粒结构示意图,该微粒的符号是________。
(2)将纯铝和铝合金相互刻划,纯铝上留下明显的划痕,说明_________。
(3)为测定某铁铝粉末混合物中铝的含量,设计了如下实验方案。
[查阅资料] Al(OH)3既可以与酸反应,也可以与碱反应生成可溶性的盐和水。Mg(OH)2不溶于水,受热分解为对应的金属氧化物和水。
[实验流程]
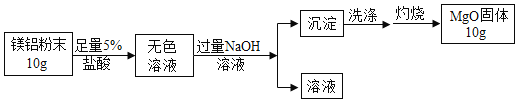
①铝与盐酸反应的化学方程式是___________。
②对沉淀进行洗涤的目的是____________。
③镁铝合金中铝的质量是_________g。
【答案】Al3+ 铝合金的硬度比纯铝的大(或其他合理答案) ![]() 除去Mg(OH)2固体表面的可溶性杂质 4
除去Mg(OH)2固体表面的可溶性杂质 4
【解析】
(1)核内质子数>核外电子数,故该微粒是铝原子失去最外层三个电子变成的铝离子,该微粒的符号是:Al3+;
(2)将纯铝和铝合金相互刻划,纯铝上留下明显的划痕,说明铝合金的硬度比纯铝大;
(3)①铝与盐酸反应生成氯化铝和氢气,该反应的化学方程式是:![]() ;
;
②对沉淀进行洗涤的目的是:除去Mg(OH)2固体表面的可溶性杂质;
③![]() ,
,![]() ,
, ,故镁全部转化到了氧化镁中,镁的质量为:
,故镁全部转化到了氧化镁中,镁的质量为:![]() ,镁铝合金中铝的质量是:10g-6g=4g。
,镁铝合金中铝的质量是:10g-6g=4g。

练习册系列答案
相关题目