题目内容
 实验室保存的-瓶浓盐酸:瓶和的标签的部分内容如图所示,请你根据标签上提供的数据回答下列问题.
实验室保存的-瓶浓盐酸:瓶和的标签的部分内容如图所示,请你根据标签上提供的数据回答下列问题.
(1)用50mL浓盐酸可以配制溶质的质量分数为10%的盐酸________g.
(2)利用刚配制好的HCI测定某二价金属的碳酸盐RC03的纯度,取样品16克(所含杂质不与酸反应,也不溶解于水),再取刚配好溶液7.3g混合至恰好反应后过滤,将溶液蒸干后得固体质量为11.1g
①该碳酸盐发生的化学方程式为________
②利用已知条件求解反应生成C02质量(x)的比例式________
③该碳酸盐化学式是________,该碳酸盐纯度为________;
④向反应后所得溶液中加入32.4g水,则此时溶液中溶质的质量分数为________.
解:(1)50×1.2×30%=18g
18g÷10%=180g;
(2)①该碳酸盐发生的化学方程式为:RCO3+2HCl=RCl2+H2O+CO2↑;
②③设生成气体的质量为x,RCl2的相对分子质量为y
RCO3+2HCl=RCl2+H2O+CO2↑
73 y 44
7.3g 11.1g x
∴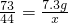 ,
,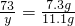
解之得:x=4.4g,y=111
因为Cl的相对原子质量为35.5,故RCl2中R的原子质量为111-35.5×2=40
对照相对原子质量表可知R是钙元素;
设样品中CaCO3的质量为z
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
z 7.3g
∴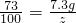
解之得:z=10g
10g÷16g×100%=62.5%,
故选CaCO3,62.5%.
④溶液质量为:10g+7.3g-4.4g+32.4g=45.3g,
溶液中溶质的质量分数为: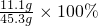 ≈24.5%.
≈24.5%.
故答案为:24.5%.
分析:(1)欲正确解答本题,需先求出50mL浓盐酸中 的溶质质量,再根据溶液质量=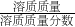 计算即可;
计算即可;
(2)①根据分数反应的物质的化学式写出反应的方程式即可;
②根据化学方程式可得出各物质的质量比,即可写出反应生成C02质量(x)的比例式;
③根据化学方程式得出各物质的质量比,写出比例式即可计算出RCl2的相对分子质量,进而计算出R的相对原子质量,即可判断该碳酸盐化学式;然后再根据化学方程式,列出比例式,即可求出样品中CaCO3的质量,根据 即可计算出样品的纯度;
即可计算出样品的纯度;
④用反应前的物质质量之和减去生成的气体的质量,计算出溶液的质量,再根据溶质质量分数= 计算即可.
计算即可.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.
18g÷10%=180g;
(2)①该碳酸盐发生的化学方程式为:RCO3+2HCl=RCl2+H2O+CO2↑;
②③设生成气体的质量为x,RCl2的相对分子质量为y
RCO3+2HCl=RCl2+H2O+CO2↑
73 y 44
7.3g 11.1g x
∴
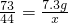 ,
,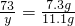
解之得:x=4.4g,y=111
因为Cl的相对原子质量为35.5,故RCl2中R的原子质量为111-35.5×2=40
对照相对原子质量表可知R是钙元素;
设样品中CaCO3的质量为z
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
z 7.3g
∴
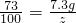
解之得:z=10g
10g÷16g×100%=62.5%,
故选CaCO3,62.5%.
④溶液质量为:10g+7.3g-4.4g+32.4g=45.3g,
溶液中溶质的质量分数为:
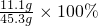 ≈24.5%.
≈24.5%.故答案为:24.5%.
分析:(1)欲正确解答本题,需先求出50mL浓盐酸中 的溶质质量,再根据溶液质量=
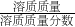 计算即可;
计算即可;(2)①根据分数反应的物质的化学式写出反应的方程式即可;
②根据化学方程式可得出各物质的质量比,即可写出反应生成C02质量(x)的比例式;
③根据化学方程式得出各物质的质量比,写出比例式即可计算出RCl2的相对分子质量,进而计算出R的相对原子质量,即可判断该碳酸盐化学式;然后再根据化学方程式,列出比例式,即可求出样品中CaCO3的质量,根据
 即可计算出样品的纯度;
即可计算出样品的纯度;④用反应前的物质质量之和减去生成的气体的质量,计算出溶液的质量,再根据溶质质量分数=
 计算即可.
计算即可.点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.

练习册系列答案
相关题目
实验室保存的一瓶浓盐酸,瓶上标签的部分内容如图所示,请你根据标签上提供的数据解答下列问题.(计算结果精确到0.01)
| 盐 酸 体积:500mL 化学式:HCl 相对分子质量:36.5 密度:1.19g/cm3 质量分数:37%(1)瓶内浓盐酸的质量是 (2)用10mL浓盐酸可以配制溶质的质量分数为10%的盐酸溶液 实验室保存的一瓶浓盐酸,瓶上标签的部分内容如图所示,请你根据标签上提供的数据解答下列问题.(计算结果精确到0.01)
(2)用10mL浓盐酸可以配制溶质的质量分数为10%的盐酸溶液________g. |