题目内容
有甲、乙、丙三种金属,将甲、乙投入硫酸铜溶液中,甲没有现象,乙的表面有红色物质析出.将丙投入甲的盐溶液中,表面没有明显变化.则甲、乙、丙三种金属活动性顺序排列正确的是( )
| A、乙>甲>丙 |
| B、乙>丙>甲 |
| C、丙>乙>甲 |
| D、丙>甲>乙 |
考点:金属活动性顺序及其应用
专题:金属与金属材料
分析:根据金属活动性顺序的应用分析解答:排在金属活动性顺序中前面的金属一般能把排在后面的金属从其盐溶液里置换出来.
解答:解:由题意可知:将甲、乙两种金属分别投入硫酸铜溶液中,乙的表面有红色物质析出,甲的表面没有明显变化,说明乙>铜>甲;将丙投入甲的盐溶液中,表面没有明显变化,说明甲>丙;则甲、乙、丙三种金属活动性顺序排列正确的乙>甲>丙;
故选A.
故选A.
点评:本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键,即在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢;位于前面的金属能把排在它后面的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
下列实验方案不正确的是( )
| A、通过观察颜色可以将NaCl溶液和KNO3溶液区分开 |
| B、加水可以将CaCO3、NH4NO3和NaOH固体区分开 |
| C、滴加肥皂水可以将蒸馏水和矿泉水区分开 |
| D、滴加酚酞溶液可以将Ca(OH)2溶液和稀硫酸区分开 |
下列哪一组结构示意图为稀有气体的原子结构示意图( )
A、 |
B、 |
C、 |
D、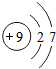 |
下列几种食品都是安徽的特产,其中糖类含量最丰富的是( )
A、 砀山梨 |
B、 萧县面皮 |
C、 长江螃蟹 |
D、 淮南豆腐 |
两瓶无色溶液分别是氯化钠和氢氧化钠溶液,下列鉴别方法中正确的是( )
| A、分别滴加酚酞试液看颜色变化 |
| B、分别加稀盐酸看现象 |
| C、取溶液蒸干,看有没有固体析出 |
| D、分别通二氧化碳后再加澄清石灰水,看有没有沉淀 |
除去下表所列物质中含有的少量杂质,所选试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质所选试剂 | 操作方法 |
| A | 二氧化碳 | 一氧化碳 | 氧气 | 点燃 |
| B | 硝酸钾溶液 | 氢氧化钾 | 氯化亚铁溶液 | 过滤 |
| C | 硫酸亚铁溶液 | 硫酸铜 | 过量的铁粉 | 过滤 |
| D | 氧化钙 | 碳酸钙 | 蒸馏水 | 溶解、过滤 |
| A、A | B、B | C、C | D、D |
 (1)饮用酸碱度过大或硬度过大的水都不利于人体健康,可用
(1)饮用酸碱度过大或硬度过大的水都不利于人体健康,可用