题目内容
在金属活动性顺序里,钠位于铜之前。某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜。该小组同学对此现象进行了如下探究:
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: 。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图:

注:煤油的密度为0.8g/mL,与水不互溶。
【解释与结论】将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,写出发生反应的化学方程式(分两步写): , 。
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: 。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图:

注:煤油的密度为0.8g/mL,与水不互溶。
| | 实验操作 | 实验现象及分析 |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 | 实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有: (任写两条)。 |
| ② | 打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 | 发生反应的化学方程式为: 。 |
| ③ | 打开止水夹c。 | 实验现象为:D中液体 ,C中产生气泡。 |
| ④ | 打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 | 实验现象为:气体燃烧,产生 色火焰。 |
| ⑤ | 在火焰上方罩一个干冷的烧杯。 | 实验现象为:烧杯内壁出现 。 |
【分析与讨论】(1)将钠与氧气和水隔绝
(2)乙 若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低
【进行实验】
【解释与结论】2Na+2H2O 2NaOH+H2↑ CuSO4+ 2NaOH Cu(OH)2↓ + Na2SO4
(2)乙 若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低
【进行实验】
| | 实验现象及分析 |
| ① | 银白色固体,熔点低,密度比水小、比煤油大等(合理即可) |
| ② | CO2+2NaOH Na2CO3+H2O |
| ③ | 倒吸入C中 |
| ④ | 淡蓝 |
| ⑤ | 无色液滴 |
试题分析:【分析与讨论】(1)由于钠化学性质非常活泼很容易和空气中的物质反应,所以常保存在煤油中,煤油的作用是将钠与氧气和水隔绝;(2)乙的猜想不合理,因为若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低【进行实验】
| | 实验现象及分析 |
| ① | 银白色固体,熔点低,密度比水小、比煤油大等(合理即可) |
| ② | CO2+2NaOH Na2CO3+H2O |
| ③ | 倒吸入C中 |
| ④ | 淡蓝 |
| ⑤ | 无色液滴 |
点评:这是一道非常典型的探究题,题目给的知识点没有学过,较为陌生,但是重点考察的反应的思想,装置等,所以这种题目不要害怕,仔细审题即可。

练习册系列答案
相关题目



 x Fe + y H2O,Fe3C + 2 H2
x Fe + y H2O,Fe3C + 2 H2 3 Fe + CH4。
3 Fe + CH4。
 3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
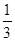 体积的NaOH溶液,发现塑料瓶变瘪。小敏宣布验证了CO2与NaOH发生了反应。
体积的NaOH溶液,发现塑料瓶变瘪。小敏宣布验证了CO2与NaOH发生了反应。

