题目内容
【题目】海水提取氯化钠的大致过程如图:

(1)图中①是_________(填“蒸发池”或“冷却池”);
(2)析出晶体后的母液是氯化钠的_________(填“饱和”或“不饱和”)溶液;
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ.溶解Ⅱ.___________(填操作名称) Ⅲ.蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是_____,该仪器在步骤Ⅲ中的作用是______。
(4)用上述实验提取的氯化钠配制100g10%的NaCl溶液,实验步骤如下:
① 计算:m(NaCl)=_________g,V(H2O)=90mL。
② 称量:分别用电子天平、量筒称量实验所需氯化钠质量和水的体积。
③ 溶解:将称量的氯化钠和水在烧杯中溶解,并用玻璃棒搅拌。
④ 装瓶:配好的溶液应装于_________(填仪器名称)中。
⑤ 贴标签:请完成所配溶液标签的书写。_____________
(5)取此氯化钠溶液测pH值,pH______7(填“>”、“<”或“=”)。
【答案】 蒸发池 饱和 过滤 玻璃棒 搅拌,使液体均匀受热,防止飞溅 细口瓶 氯化钠溶液 10% =
【解析】(1)氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离,故图中①是蒸发池;(2)析出晶体后的母液,不能溶解溶解氯化钠,为氯化钠的饱和溶液;(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:溶解、过滤、蒸发;上述三个步骤中,用到的同一种玻璃仪器的名称是玻璃棒,该仪器在步骤Ⅲ中的作用是:溶解时的作用是搅拌;过滤是的作用是引流;蒸发时的作用是搅拌,使液体均匀受热,防止飞溅;(4) ①配制100g溶质质量分数为3%的氯化钠溶液,需要氯化钠的质量为100g×3%=3g;④ 装瓶:配好的溶液应装于细口瓶中;⑤ 贴标签:氯化钠溶液,10%;(5)氯化钠溶液为中性溶液,故PH=7。

【题目】阅读下面科普短文(原文有删改)
食盐
食盐是生活中常用的调味品,主要成分是氯化钠,在人体中有调节水分、维持酸碱平衡等生理作用。
资料一:食盐的加工
工业上用海水晒盐或用盐湖水、盐井水煮盐,使氯化钠晶体析出。这样制得的氯化钠含有较多的杂质,称为粗盐。粗盐经下图所示主要流程可成为精盐。

资料二:食盐的种类
市面上食盐制品种类繁多,现简要介绍几种。原盐,即粗盐,常用于腌制工艺;精盐,由粗盐提纯而成,适合烹饪调味;碘盐,在食盐中添加一定量碘酸钾(KIO3)即为碘盐,可防治碘缺乏病;低钠盐,食盐中添加氯化钾、硫酸镁等有“咸味”的成分,可防治因钠离子摄入过多而引起的高血压等疾病。
资料三:食盐的摄入量
虽然我们的身体离不开食盐,但摄入过多也会对身体产生危害。按照世界卫生组织的推荐标准,成人每天食盐摄入量不宜超过6g。然而据调查,我国人均每天的食盐摄入量为9.1g。一方面三餐中食盐量需要控制,另一方面,许多成品食物中食盐的含量也应引起重视,下表所示为部分成品食物每100g中的食盐含量。
食品 | 某品牌方便面 | 某品牌酱油 | 某品牌薯片 |
食盐含量g/100g | 3 | 16 | 1.6 |
依据文章内容回答下列问题。
(1)由粗盐制得精盐的过程属于_________(填“物理”或“化学”)变化。
(2)成人每天食盐摄入量不宜超过_____________g。
(3)如果某人一天吃了两袋(共300g)上表中所示方便面,按照世界卫生组织推荐标准,其当天食盐摄入量________(填“超标”或“未超标”)。
(4)下列关于食盐的说法正确的是_________。
A.高血压患者,可适当选择低钠盐
B.目前我国居民食盐摄入量普遍偏高
C.氯化钠是维持人体生命活动的重要物质
D.为补充人体所需钠元素和氯元素,每天做饭时可加入大量食盐
(5)请你为人们提一条日常摄取食盐的建议:_________________________。
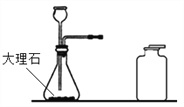
【题目】某小组对石灰石进行煅烧,并对煅烧后固体成分进行探究。
(1)写出此反应的化学方程式_______________________。 (2)根据化学方程式进行猜想。固体残留物成分: I. 只有氧化钙;II. 只有碳酸钙;III. _____________ (3)甲乙丙三位同学分别设计了三种方案探究煅烧后固体成分。 友情提示:①CaO+2HCl→CaCl2+H2O; ②Ca(OH)2+2HCl→CaCl2+2H2O ③氯化钙溶液呈中性。 | |||||
方案设计 | 操作及现象 | 实验结论 | 解释 | ||
方案一 |
| 固体物质中 一定含有_______ | 用化学方程式解释判断理由_______。 | ||
方案二 |
| 乙同学得出 猜想II成立 | 该同学设计方案是否合理,理由是______。 | ||
方案三 |
| 猜想III成立 | |||
【题目】水是生命的源泉,也是不可缺少的资源。
(1)某矿泉水的主要矿物质成分及含量如下表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指________ (填“单质、元素、分子或原子”)。
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:
(Ⅰ)自来水、蒸馏水、海水中属于纯净物的是___________。
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如下图所示:

①对应的作用是_________(填字母序号,下同),③对应的作用是_______。
A. 杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏