题目内容
【题目】请结合下列实验常用装置,回答有关问题。

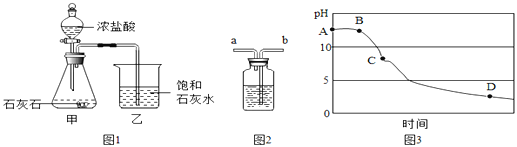
(1)写出仪器a的名称__________。
(2)实验室用氯酸钾和二氧化锰制取氧气,可采用的发生装置为_______,发生反应的化学方程式是__________。若改用高锰酸钾制取氧气,发生装置应作的改动是_________。
(3)实验室制取二氧化碳的化学方程式为__________________________,若要制取一瓶二氧化碳,可采用的装置组合为_________,向集气瓶中倒入澄清石灰水,发现澄清石灰水溶液不变浑浊,造成这一现象的可能原因是____________________,若要使反应停止可采取的操作是__________________________。
(4)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置I中产生气体的化学方程式为:H2SO4(浓)+Na2SO3═Na2SO4+SO2↑+H2O

①装置Ⅱ中生成Na2S2O5晶体发生的是化合反应,其反应的化学方程式为:____________。
②Na2S2O5中硫元素的化合价是_____________。
③装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为___________(填序号)。

【答案】 水槽 A 2KClO3 ![]() 2KCl+3O2↑ 试管口塞一团棉花 CaCO3+2HCl=CaCl2+H2O+CO2↑ CD 装置漏气或石灰水变质或CO2中混有HCl气体 关闭活塞 Na2SO3+SO2=Na2S2O5 +4 d
2KCl+3O2↑ 试管口塞一团棉花 CaCO3+2HCl=CaCl2+H2O+CO2↑ CD 装置漏气或石灰水变质或CO2中混有HCl气体 关闭活塞 Na2SO3+SO2=Na2S2O5 +4 d
【解析】(1)根据常见仪器解答;(2)根据氯酸钾在二氧化锰的催化并加热的条件下分解生成氯化钾和氧气及用高锰酸钾加热需在试管口放一团棉花解答;(3)根据碳酸钙与盐酸常温下反应生成氯化钙、二氧化碳和水及实验过程中的注意事项分析解答;(4) ①根据亚硫酸钠与二氧化硫反应生成焦亚硫酸钠解答;②根据化合物中各元素正负化合价代数和为0解答,③根据处理过量的SO2尾气,既要吸收SO2尾气,同时能防倒吸解答。(1)仪器a的名称水槽;(2)实验室用氯酸钾和二氧化锰在加热的条件下制取氧气,可采用的发生装置为A,发生反应的化学方程式是2KClO3 ![]() 2KCl+3O2↑;若改用高锰酸钾制取氧气,发生装置应作的改动是在试管口塞一团棉花;(3)碳酸钙与盐酸常温下反应生成氯化钙、二氧化碳和水,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;若要制取一瓶二氧化碳,可采用的装置组合为CD;向集气瓶中倒入澄清石灰水,发现澄清石灰水溶液不变浑浊,造成这一现象的可能原因是装置漏气(或石灰水变质或CO2中混有HCl气体);若要使反应停止可采取的操作是关闭活塞;(4) ①亚硫酸钠与二氧化硫反应生成焦亚硫酸钠,反应的化学方程式为Na2SO3+SO2=Na2S2O5;②Na2S2O5中钠元素显-1价,氧元素显-2价。Na2S2O5中硫元素的化合价是{0-[(+1×2)+(-2×5)]}÷2=+4;③处理过量的SO2尾气,a、装置应将导管伸入到氨水中可以吸收二氧化硫,但为密闭环境,装置内压强增大,易产生安全事故,错误;b、食盐水不能将大量的SO2尾气吸收,且为密闭环境,装置内压强增大,易产生安全事故,错误;c、该装置不能吸收二氧化硫,无法实现实验目的,错误,d、氢氧化钠溶液可吸收SO2尾气,同时能防倒吸,正确。故选d。
2KCl+3O2↑;若改用高锰酸钾制取氧气,发生装置应作的改动是在试管口塞一团棉花;(3)碳酸钙与盐酸常温下反应生成氯化钙、二氧化碳和水,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;若要制取一瓶二氧化碳,可采用的装置组合为CD;向集气瓶中倒入澄清石灰水,发现澄清石灰水溶液不变浑浊,造成这一现象的可能原因是装置漏气(或石灰水变质或CO2中混有HCl气体);若要使反应停止可采取的操作是关闭活塞;(4) ①亚硫酸钠与二氧化硫反应生成焦亚硫酸钠,反应的化学方程式为Na2SO3+SO2=Na2S2O5;②Na2S2O5中钠元素显-1价,氧元素显-2价。Na2S2O5中硫元素的化合价是{0-[(+1×2)+(-2×5)]}÷2=+4;③处理过量的SO2尾气,a、装置应将导管伸入到氨水中可以吸收二氧化硫,但为密闭环境,装置内压强增大,易产生安全事故,错误;b、食盐水不能将大量的SO2尾气吸收,且为密闭环境,装置内压强增大,易产生安全事故,错误;c、该装置不能吸收二氧化硫,无法实现实验目的,错误,d、氢氧化钠溶液可吸收SO2尾气,同时能防倒吸,正确。故选d。

【题目】除去下列物质中混有的杂质,所用试剂和操作方法不正确的是![]()
物质 | 所含杂质 | 除杂质选用的试剂或方法 | |
A | NaCl溶液 | NaOH | 滴加适量的稀盐酸 |
B | Cu | Fe | 加入足量的稀盐酸并过滤 |
C |
| CO | 在氧气中点燃 |
D |
|
| 加入足量的水溶解并过滤、洗涤、干燥 |
A. A B. B C. C D. D