题目内容
 (2011?仪征市一模)在宏观、微观和符号之间建立联系是化学学科的特点.
(2011?仪征市一模)在宏观、微观和符号之间建立联系是化学学科的特点.(1)在水、铜和氯化钠3种物质中,由分子构成的是
水
水
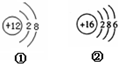
;(2)如图为两种微粒结构示意图,其中属于离子的是
①
①
;(3)今年日本因地震、海啸而引发的核爆炸造成了严重核污染,其中放射性核素碘-131已飘至我国,它与加碘食盐中碘-127因质子数相同而同属碘元素,则碘-131原子与碘-127原子的差异是
中子数
中子数
(选填“质子数”、“中子数”或“电子数”)不同.(4)实验室常用过氧化氢溶液和二氧化锰制取氧气,发生反应的化学反应方程式为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,在这个化学变化过程中,最小的粒子是
| ||
氢原子和氧原子
氢原子和氧原子
.分析:(1)根据金属和大多数固态非金属单质等由原子构成,有些物质是由分子构成的,如水、气态非金属单质等,有些物质是由离子构成的,如氯化钠,进行分析解答即可.
(2)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
(3)根据题意,碘-131与加碘食盐中碘-127因质子数相同而同属碘元素,根据元素的概念进行分析判断.
(4)根据实验室制取氧气的反应原理写出反应的化学方程式,与原子的概念进行分析解答即可.
(2)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
(3)根据题意,碘-131与加碘食盐中碘-127因质子数相同而同属碘元素,根据元素的概念进行分析判断.
(4)根据实验室制取氧气的反应原理写出反应的化学方程式,与原子的概念进行分析解答即可.
解答:解:(1)水是由水分子构成;铜属于金属,是由铜原子直接构成的;氯化钠是由钠离子和氯离子构成的.
(2)①质子数=12,核外电子数=10,质子数>核外电子数,为阳离子;②质子数=核外电子数=16,为原子,故选项错误.
(3)根据题意,碘-131与加碘食盐中碘-127因质子数相同而同属碘元素,它们的核内质子数相同,核外电子数相同,核内中子数不同.
(4)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
2H2O+O2↑;原子是化学变化中的最小粒子,过氧化氢分子是由氢原子和氧原子构成的,故在这个化学变化过程中,最小的粒子是氢原子和氧原子.
故答案为:(1)水;( 2)①;(3)中子数;(4)2H2O2
2H2O+O2↑;氢原子和氧原子.
(2)①质子数=12,核外电子数=10,质子数>核外电子数,为阳离子;②质子数=核外电子数=16,为原子,故选项错误.
(3)根据题意,碘-131与加碘食盐中碘-127因质子数相同而同属碘元素,它们的核内质子数相同,核外电子数相同,核内中子数不同.
(4)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
| ||
故答案为:(1)水;( 2)①;(3)中子数;(4)2H2O2
| ||
点评:本题难度不大,掌握常见物质的粒子构成、核内质子数和核外电子数之间的关系、原子的构成、化学方程式的书写等即可正确解答本题.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
 (2011?仪征市一模)一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.工业上常用天然气和水蒸气或二氧化碳经高温催化反应得到CO和H2,得到的CO和H2的混合气被称为合成气.如图为利用合成气合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程.
(2011?仪征市一模)一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.工业上常用天然气和水蒸气或二氧化碳经高温催化反应得到CO和H2,得到的CO和H2的混合气被称为合成气.如图为利用合成气合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程.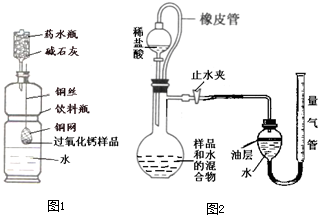 (2011?仪征市一模)长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体,为鱼提供氧气,过氧化钙与水反应除生成氧气外,还生成什么物质?课外兴趣小组决定对这一过程中进行探究:
(2011?仪征市一模)长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体,为鱼提供氧气,过氧化钙与水反应除生成氧气外,还生成什么物质?课外兴趣小组决定对这一过程中进行探究: