题目内容
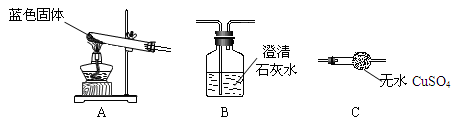
(8分)实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如右图所示)。实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中。

(1)甲同学的实验中向 中滴加石蕊试液后,溶液颜色为红色。
(2)甲组同学将两支试管中的液体混合后,烧杯A中的溶液溶质一定有 。
A.HCl B.NaOH C.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
,② ,③ 。
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
(4)最后,两位同学向烧杯C中加入 ,实现了此次实验的绿色排放(呈中性)。

(1)甲同学的实验中向 中滴加石蕊试液后,溶液颜色为红色。
(2)甲组同学将两支试管中的液体混合后,烧杯A中的溶液溶质一定有 。
A.HCl B.NaOH C.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
,② ,③ 。
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
| 操作方法 | 实验现象 | 实验结论 |
| | | |
(4)最后,两位同学向烧杯C中加入 ,实现了此次实验的绿色排放(呈中性)。
(1)HCl或稀盐酸。(2)BC(3)【猜想与假设】①NaCl、NaOH ②NaCl、NaOH、Ca(OH)2 ③NaCl、NaOH、Na2CO3 【设计完成实验】(其他答案合理给分)
(4)适量稀盐酸(或加入稀盐酸至溶液由蓝色变为紫色)
| 操作方法 | 实验现象 | 实验结论 |
| ①取少量C中废液于试管中,加入适量稀盐酸 ②另取少量C中废液于试管中,加入碳酸钠溶液 | 若有气泡产生 若有沉淀产生, 若两支试管均无现象 | 则C中废液的成分是NaCl、NaOH、Na2CO3 则C中废液的成分是 NaCl、NaOH、Ca(OH)2 则C中废液的成分是NaCl、NaOH |
(4)适量稀盐酸(或加入稀盐酸至溶液由蓝色变为紫色)
试题分析:由现象可知(1)甲同学的实验中向盐酸中滴加石蕊试液后,溶液颜色为红色。操作的现象知溶液中含有碱(2)甲组同学将两支试管中的液体混合后,烧杯A中的溶液溶质一定有氯化钠和氢氧化钠;(3)两位同学继续对烧杯C中的废液成分进行探究,【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,根据反应的程度,知其组成可能为:【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:①NaCl、NaOH ②NaCl、NaOH、Ca(OH)2 ③NaCl、NaOH、Na2CO3【设计完成实验】为:
| 操作方法 | 实验现象 | 实验结论 |
| ①取少量C中废液于试管中,加入适量稀盐酸 ②另取少量C中废液于试管中,加入碳酸钠溶液 | 若有气泡产生 若有沉淀产生, 若两支试管均无现象 | 则C中废液的成分是NaCl、NaOH、Na2CO3 则C中废液的成分是 NaCl、NaOH、Ca(OH)2 则C中废液的成分是NaCl、NaOH |

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目

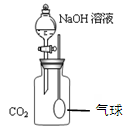
 方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。