题目内容
【题目】根据所学化学知识回答下列问题。
①天然气的主要成分是甲烷(CH4),甲烷属于______(选填“有机”或“无机”)物,其中碳元素以____(选填“游离”或“化合”)态存在;甲烷完全燃烧的化学方程式是___。
②自来水厂净水过程中除去色素和异味用到活性炭,主要利用其______性。
③“中国芯”彰显中国“智”造。芯片的基材主要是高纯硅,工业上利用三氯硅烷(HSiCl3)制取高纯硅。三氯硅烷含有_____种元素,1mol HSiCl3中约含______个氯原子。
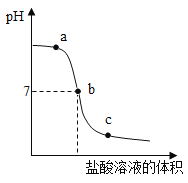
④某工业品盐酸的溶质质量分数为37%。“37%”的含义是_____;要配制100g 7.4%的稀盐酸,需要37%的盐酸____g。
【答案】有机 化合 CH4 +2O2![]() CO2 + 2H2O 吸附 3 1.806 ×1024 在100g盐酸(或在100g溶液)中含氯化氢37g 20
CO2 + 2H2O 吸附 3 1.806 ×1024 在100g盐酸(或在100g溶液)中含氯化氢37g 20
【解析】
①天然气的主要成分是甲烷(CH4),是含碳的化合物,甲烷属于有机物,其中碳元素以化合态存在;甲烷完全燃烧生成二氧化碳和水,化学方程式是CH4 +2O2![]() CO2 + 2H2O;
CO2 + 2H2O;
②自来水厂净水过程中除去色素和异味用到活性炭,主要利用其吸附性;
③工业上利用三氯硅烷(HSiCl3)制取高纯硅。三氯硅烷含有三种元素,一个三氯硅烷分子中有3个氯原子,1mol HSiCl3中约含6.02×1023个分子,故含有1.806 ×1024个氯原子;
④某工业品盐酸的溶质质量分数为37%。![]() , “37%”的含义是在100g盐酸(或在100g溶液)中含氯化氢37g;要配制100g 7.4%的稀盐酸,设需要37%的盐酸的质量为x,则:100g ×7.4%=37%x,x=20g。
, “37%”的含义是在100g盐酸(或在100g溶液)中含氯化氢37g;要配制100g 7.4%的稀盐酸,设需要37%的盐酸的质量为x,则:100g ×7.4%=37%x,x=20g。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
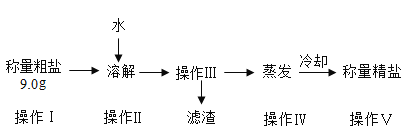
同步拓展阅读系列答案【题目】某小组同学欲提纯粗盐(只含氯化钠和少量泥沙)样品,实验过程和氯化钠的溶解度数据如下。
温度(°C) | 10 | 20 | 30 | 40 | 60 |
溶解度/g/100g水 | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 |
(1)30°C时氯化钠的溶解度是______________。
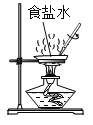
(2)操作Ⅲ的名称是______________,其原理是依据_____________的性质进行提纯。
(3)最终提纯所得精盐质量偏少,可能的原因是______________ (选填编号)。
a 操作II中食盐未完全溶解就进行操作Ⅲ
b 操作Ⅲ中有滤渣漏入承接液体的烧杯
c 操作II、IV实验过程中有物质溅出
d 操作IV蒸发最终所得精盐比较潮湿
(4)溶解粗盐时,加入20°C水合适的量约为_____________(选填“20”、“30” 或“50”) mL。
(5)称取4.5g提纯的精盐,可配制质量分数为0.9%的食盐溶液______________g。