题目内容
向10g铜和氧化铜的混合物中逐滴滴入溶质质量分数为9.8%的稀硫酸至恰好完全反应,测得共用去稀硫酸100g,过滤。计算:
(1)原混合物中铜元素的质量为多少克?
(2)过滤后所得溶液的溶质质量分数。
(1) 8.4g (2)14.8%
解析试题分析:本题难度适中。铜做为不活泼金属不会和稀硫酸反应,氧化铜能与稀硫酸反应生成硫酸铜,题目未告知铜和氧化铜的质量,我们只能依据恰好完全反应从反应的硫酸的质量计算出氧化铜和硫酸铜的质量。必须注意的是(1)提问是铜元素的质量,氧化铜中也含有铜元素质量不可忽视,所以质量为10g-8g+(8*(64/80))g=8.4g;过滤后溶液的溶质为硫酸铜,质量是16g,可溶液质量必须注意,不是100+10=110g,因为原来混合物中铜单质2g没有参与反应,过滤也除去了,所以溶液质量为100+8=108g,因而进一步得到答案是(16g/(100g+8g))*100%=14.8%。
解:稀硫酸中参加反应的硫酸质量为100g×9.8%=9.8g
设:反应产生的CuSO4是xg,反应消耗的CuO为yg.
CuO+ H2SO4 = CuSO4 + H2O
80 98 160
y 9.8g x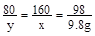
x="16g"
y=8g
10g-8g+(8*(64/80))g=8.4g
(16g/(100g+8g))*100%
= 14.8%
答:铜元素的质量为8.4g ,过滤后所得溶液的溶质质量分数为14.8%
考点:化学方程式的计算及溶液的质量分数计算。
点评:溶液的质量分数一直会是计算的重点。

为测定混有少量氯化钠的碳酸钠固体中碳酸钠的质量分数,向盛有12g该混合物的烧杯中加入过量稀盐酸至碳酸钠完全反应。
反应过程用精密仪器测得烧杯和药品的质量与反应时间的数据记录如下:
| 反应时间 | t0 | t1 | t2 | t3 | t4 | t5 |
| 烧杯和药品质量/g | 210.0 | 206.7 | 205.9 | 205.6 | 205.6 | 205.6 |
(1)则完全反应后,生成二氧化碳的质量。
(2)请计算混合物中碳酸钠的质量分数(精确到0.1%)。
(3)假如称量准确,通过计算得到的碳酸钠的质量分数比实际数值偏小,其原因是 。
实验室将10g质量分数为98%的硫酸稀释成10%的稀硫酸,需要水的质量为( )
| A.49g | B.88g | C.98g | D.100g |
自然界有一种含镁矿石,其化学组成可表示为 xMgCO3 ? yMg(OH)2(x、y 为正整数) 。取两份等质量的样品,一份加过量盐酸生成气体8.8g;另一份加热至完全分解得到固体 MgO 的质量为 10g(MgCO3? MgO+CO2↑;Mg(OH)2? MgO+H2O) 。下列x,y 的关系正确的是
| A.x∶y=4∶1 | B.x∶y =1∶4 | C.x∶y=1∶1 | D.x∶y=2∶1 |
 CaO+CO2↑)
CaO+CO2↑)