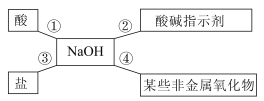
题目内容
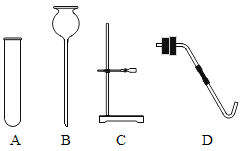
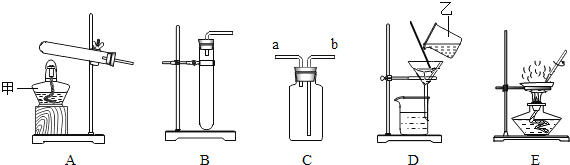
【题目】实验是进行科学探究的主要方法。下图是初中化学常见实验装置。请回答:
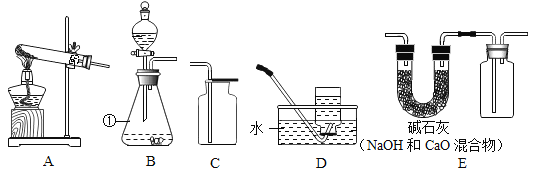
(1)装置中仪器①的名称为_____。
(2)若选用A装置来制取氧气,则反应的化学方程式为_____。
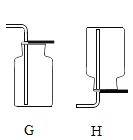
(3)①实验室常用大理石和稀盐酸反应制取CO2,反应的化学方程式为_____。制取并收集CO2可选用的装置组合是_____(填字母)。
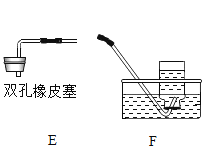
②若用E装置干燥并收集一瓶某气体,则该气体可能是_____(填字母)。
A CO2
B O2
C H2
D NH3
(4)实验室可用块状电石(CaC2) 与足量的水在常温下剧烈反应制取乙炔(C2H2)气体,该反应的化学方程式是_____。图中适合制取乙炔气体的发生装置是_____(填字母)。
(5)小雨同学在探究Al、Fe、Cu三种金属的活动性实验时,设计了如下方案:
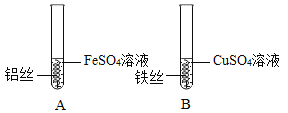
①小雨在很长时间内都未观察到A试管中预期的实验现象,从操作上分析可能的原因是_____。
②实验成功后,小雨把两支试管中所有物质合并,然后倒入烧杯中,充分反应后,烧杯中仍有不溶性固体。为此,小雨继续展开探究。
[提出问题]不溶性固体中含有哪些成分?
[实验并得出结论]过滤,向滤出的不溶性固体中滴加足量的稀硫酸,有气泡冒出,则该不溶性固体中一定含有的物质是_____,此时一定发生反应的化学方程式是_____。
③[反思与评价]小军同学用表面积相等的以上三种金属片分别与等浓度等体积的稀盐酸反应完成同样的探究,却意外发现铁片中加稀盐酸后,溶液变为黄色。试写出溶液变为黄色的化学方程式_____。
【答案】锥形瓶 ![]() CaCO3+2HCl=CaCl2+ H2O+ CO2↑ BC B CaC2+2H2O=C2H2+Ca(OH)2 B 未将铝丝表面的氧化膜除去 铁和铜(或Fe和Cu) Fe+ H2SO4=FeSO4+H2↑ 6HCl+Fe2O3=2FeCl3+3H2O
CaCO3+2HCl=CaCl2+ H2O+ CO2↑ BC B CaC2+2H2O=C2H2+Ca(OH)2 B 未将铝丝表面的氧化膜除去 铁和铜(或Fe和Cu) Fe+ H2SO4=FeSO4+H2↑ 6HCl+Fe2O3=2FeCl3+3H2O
【解析】
(1)装置中仪器①的名称为:锥形瓶。
(2)高锰酸钾固体加热制取氧气时,为了防止高锰酸钾粉末随氧气流进入导气管,试管口要放一团棉花,题中A装置试管口有一团棉花,若选用A装置来制取氧气,则反应物是高锰酸钾,反应的化学方程式为:![]() 。
。
(3)①大理石(主要成分是碳酸钙)和稀盐酸反应生成氯化钙、水和CO2,实验室用大理石和稀盐酸反应制取CO2,反应的化学方程式为:CaCO3+2HCl=CaCl2+ H2O+ CO2↑。因为反应物是固体和液体,反应不需要加热,所以发生装置选择B;二氧化碳密度比空气大,能溶于水,不能用排水法收集,只能用向上排空气法收集,因此收集装置选择C,故制取并收集CO2可选用的装置组合是:BC。
②E装置中干燥剂是碱石灰,二氧化碳能跟氢氧化钠反应,二氧化碳还能和氧化钙吸水后生成的氢氧化钙反应,因此不可以用E装置干燥二氧化碳;O2不跟碱石灰中的成分反应,碱石灰能吸收氧气中的水分,且氧气的密度比空气略大,用该集气瓶收集氧气应从左侧长导管进,因此该装置可以干燥并收集一瓶氧气;H2、NH3都可以用碱石灰干燥,但因为密度比空气小,用该集气瓶收集这两种气体应该从右侧短导管进,不可用图中装置收集。因此若用E装置干燥并收集一瓶某气体,则该气体可能是:B。
(4)实验室可用块状电石(CaC2) 与足量的水在常温下剧烈反应制取乙炔(C2H2)气体,同时生成氢氧化钙,该反应的化学方程式是:CaC2+2H2O=C2H2+Ca(OH)2。因为反应物是固体和液体,反应不需要加热,故图中适合制取乙炔气体的发生装置是:B。
(5)①实验中小雨在很长时间内都未观察到A试管中预期的实验现象,从操作上分析可能的原因是:没有除去铝丝表面的氧化膜。因为铝的化学性质比较活泼,铝丝在空气中很容易跟氧气反应生成一层致密的氧化铝薄膜,所以不将该氧化膜打磨除去,铝就不能和硫酸亚铁溶液接触反应。
②实验成功后,小雨把两支试管中所有物质合并,然后倒入烧杯中,充分反应后,烧杯中仍有不溶性固体。
实验并得出结论:过滤,向滤出的不溶性固体中滴加足量的稀硫酸,有气泡冒出,说明固体中一定含有金属活动性顺序中排在氢前面的金属,溶液中的铜全部被置换出来,又因为铝比铁活泼,所以固体中一定有铁可能有铝,则该不溶性固体中一定含有的物质是:铁和铜(或Fe和Cu)。该实验中一定发生铁和稀硫酸的反应,化学方程式是:Fe+ H2SO4=FeSO4+H2↑。
③反思与评价:因为铁片容易生锈,铁锈的主要成分是氧化铁,氧化铁和稀盐酸反应生成氯化铁溶液,溶液呈黄色,而铁与稀盐酸反应生成氯化亚铁溶液时,氯化亚铁溶液呈浅绿色,所以铁片中加稀盐酸后溶液变为黄色的化学方程式是:6HCl+Fe2O3=2FeCl3+3H2O。

 一本好题口算题卡系列答案
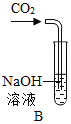
一本好题口算题卡系列答案【题目】对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究 CO2 通入NaOH 溶液是否发生了反应,设计了下列二组实验。请和化学兴趣小组的同学一起探究并回答问题:
(设计与实验)
实验序号 | 实验步骤一 | 实验步骤二 | 实验序号 | 实验步骤一 | 实验步骤二 |
实验 I |
|
| 实验II |
|
|
(探究与结论)
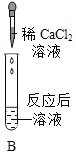
(1)实验I中步骤一看不到明显现象,步骤二产生的现象是_____。
(2)实验Ⅱ中步骤二发生的化学方程式是_____,其中CaCl2溶液也可以用_____(填字母)代替达到实验目的。
A 硝酸钡溶液 B 氯化钾溶液 C 碳酸钾溶液 D 硫酸钠溶液
(3)在实验Ⅱ的步骤一中CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是_____。
(拓展延伸)现有下列信息:

请你和化学兴趣小组的同学一起利用以上资料信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
实验Ⅲ的操作为:_____。看到的现象是_____。
【题目】工业上常利用电石制乙炔气体![]() 时产生的灰浆和残渣制备化工原料
时产生的灰浆和残渣制备化工原料![]() 和超细
和超细![]() .
.
![]() 电石制乙炔气体
电石制乙炔气体![]() 时产生灰浆和残渣的过程如下:电石
时产生灰浆和残渣的过程如下:电石![]() 灰浆
灰浆![]() 残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是
残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是![]() 和 ______ .
和 ______ .
Ⅰ![]() 制备
制备![]() 的流程如图:
的流程如图:
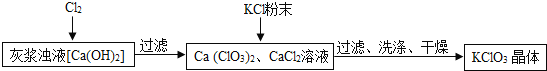
![]() 向灰浆浊液中通入
向灰浆浊液中通入![]() ,得到
,得到![]() 、
、![]() 溶液.反应中
溶液.反应中![]() 与
与![]() 的化学计量数分别为1和
的化学计量数分别为1和![]() 写出此反应的化学方程式 ______ .
写出此反应的化学方程式 ______ .
![]() 有关物质在常温下的溶解度如下:
有关物质在常温下的溶解度如下:
物质 |
|
|
| KCl |
溶解度 |
|
|
|
|
上述流程中加入KCl粉末,KCl与 ______ ![]() 填化学式
填化学式![]() 发生了复分解反应,得到
发生了复分解反应,得到![]() 晶体.你认为能得到
晶体.你认为能得到![]() 晶体的原因是 ______ .
晶体的原因是 ______ .
![]() 洗涤时,可选用下列洗涤剂 ______
洗涤时,可选用下列洗涤剂 ______ ![]() 填字母编号
填字母编号![]() .
.
A KCl饱和溶液![]() 冰水
冰水![]() 饱和
饱和![]() 溶液
溶液
Ⅱ![]() 制备超细
制备超细![]() 的流程如下
的流程如下![]() 注:加入
注:加入![]() 溶液的目的是溶解残渣中的难溶盐
溶液的目的是溶解残渣中的难溶盐![]() :
:
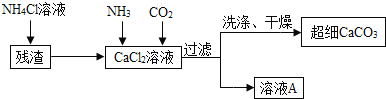
![]() 向
向![]() 溶液中通入两种气体,生成超细
溶液中通入两种气体,生成超细![]() 的化学方程式 ______
的化学方程式 ______ ![]() 检验
检验![]() 是否洗涤干净的方法是 ______ .
是否洗涤干净的方法是 ______ .
![]() 流程中溶液A可循环使用,其主要成分的化学式是 ______ .
流程中溶液A可循环使用,其主要成分的化学式是 ______ .
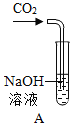
【题目】(1)实验室制取二氧化碳是中学化学的一个重要实验,同学们在制出二氧化碳后又进行了相关的系列实验,实验装置如图:

①B装置中反应的化学方程式为_____________________。
②用A装置制气体的最大优点是___________________。
③C装置的作用是__________________,D装置的作用是___________________。
④E装置中发生反应的实验现象为___________________。
⑤F装置除了吸收CO2外,还可以起到的作用是___________________。
(2)在化学实验探究课上,化学老师交给某学习小组一包白色粉末,并提示该粉末由Na2SO4、NaNO2(亚硝酸钠)、NaCl 中的一种或几种组成。该小组同学们探究该白色粉末组成的实验过程如下:
[查阅资料]1亚硝酸盐能溶于水
2Na2SO4、NaNO2、NaCl的部分性质如表:
化学式 | 水溶液的酸碱性 | 与稀盐酸作用 | 毒性 |
NaNO2 | 碱性 | 产生棕红色气体 | 有 |
NaCl | 中性 | 不反应 | 无 |
Na2SO4 | 中性 | 不反应 | 无 |
[实验探究]
限用以下试剂:蒸馏水、酚酞试液、氯化钡溶液、硝酸钡溶液、硝酸银溶液、稀盐酸、稀硝酸
步骤 | 实验操作 | 实验现象 | 实验结论 |
步骤一 | 取少量白色粉末加入试管中,加蒸馏水溶解,滴加____________。 | 无现象 | 白色粉末中不含有NaNO2 |
步骤二 | 另取少量白色粉末加入试管中,加蒸馏水溶解,______________。 | _____________ | 白色粉末中含有Na2SO4和NaCl |
步骤三 | _______________ | _____________ |