题目内容
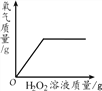
【题目】小亮做了“铁在氧气里燃烧”的实验,铁丝在氧气中燃烧的化学方程式为_______,实验结束后,他想对得到的黑色固体做进一步探究。于是他查阅资料,并在老师的指导下进行了以下探究活动:
(查阅资料)
①自然界中铁的氧化物主要是Fe3O4和Fe2O3,FeO在空气中极易被氧化成Fe2O3;②Fe3O4和Fe2O3的分解温度、铁的熔点见表:
物质名称 | Fe3O4 | Fe2O3 | Fe |
分解温度/℃ | 1538 | 1400 | |
熔点/℃ | 1535 |
(提出猜想)黑色固体的成分是:
猜想I:Fe和Fe3O4; 猜想II:只有_______;
猜想III:Fe3O4和FeO;猜想IV:只有FeO。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
将黑色固体碾碎,露置在空气中。 | _______。 | 猜想III、IV不成立。 |
将黑色固体碾碎,加入盛硫酸铜溶液的试管中。 | 有红色物质生成。 | 猜想______成立。 |
(实验分析)
(1)做铁丝燃烧的实验前,集气瓶内需要_______。
(2)实验过程中加硫酸铜溶液反应的化学方程式为_______:。
(3)根据实验现象和表中数据,可知铁在氧气里燃烧时产生的高温应在_______之间,铁在氧气里燃烧产生的是Fe3O4而不是Fe2O3的原因是: _______。
【答案】![]() Fe3O4 黑色固体不变红 I 装少量的水(或铺一层薄细沙) Fe+CuSO4=Cu+FeSO4 1535℃~1538℃ 此温度范围氧化铁已分解
Fe3O4 黑色固体不变红 I 装少量的水(或铺一层薄细沙) Fe+CuSO4=Cu+FeSO4 1535℃~1538℃ 此温度范围氧化铁已分解
【解析】
铁丝在氧气中燃烧生成四氧化三铁,反应的化学方程式为:![]() ;
;
[提出猜想]
猜想Ⅰ:Fe和Fe3O4;猜想Ⅱ:只有Fe3O4;猜想Ⅲ:Fe3O4和FeO;猜想Ⅳ:只有FeO。
[实验探究]
将黑色固体碾碎,露置在空气中将黑色固体,黑色固体不变色,说明黑色固体中不含有氧化亚铁,猜想III、IV不成立。
碾碎,加入盛硫酸铜溶液的试管中,产生红色固体,是因为铁和硫酸铜反应生成了铜,猜想I成立。
[实验分析]
(1)做铁丝燃烧的实验前,集气瓶内需要加入适量水或铺一层细沙,以防止高温熔融物溅落时炸裂集气瓶。
(2)实验过程中加硫酸铜溶液时,铁和硫酸铜反应生成了铜和硫酸亚铁,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu。
(3)根据实验现象和表中数据可知,铁在氧气里燃烧时产生的高温应大于铁的熔点,而小于四氧化三铁的分解温度,即在1535℃~1538℃之间;
铁在氧气里燃烧产生的是Fe3O4的原因是铁在氧气里燃烧产生的高温能使氧化铁分解。

【题目】据媒体报道某家长带小孩在下水道井盖小孔上点燃鞭炮后,投入下水道内,发生爆炸。同学们对此很好奇并要探究某下水道的气体的成分:(提示:氢氧化钠溶液能充分吸收二氧化碳)
(猜想)Ⅰ含有可燃性气体CO; Ⅱ含有可燃性气体CH4; Ⅲ含有可燃性气体CO和CH4;
(收集气体)用大的可乐塑料瓶装满水,打开瓶盖用绳子吊入下水道中,用铁钩将矿泉水瓶倒转,使水倒出,将瓶提到井口迅速盖好瓶盖备用,该方法是_______法收集气体。
(进行实验)
步骤 | 实验操作 | 实验现象 | 结论 |
(1) | 导出瓶中气体,通过装有氢氧化钠溶液的洗气瓶 | 目的是除去二氧化碳等酸性气体 | |
(2) | 再通过装有浓硫酸的洗气瓶 | 目的是除去__________ | |
(3) | 将步骤(2)的气体导出点燃 ①用干燥且冷的烧杯罩在火焰上方 ②用内壁附有澄清石灰水的烧杯罩在火焰上方 | ①烧杯内壁_______________ ②烧杯内壁变浑浊 | ①证明该气体中一定含有氢元素 ②证明该气体中一定含有___元素 |
(作出判断)根据上述实验现象,甲同学认为猜想Ⅲ正确,而乙同学认为甲的判断不严谨。因为猜想_________也有相同的现象。如需进一步确认还应检验___________的存在。利用其化学性质检验的方法是______(用化学方程式表示)
(拓展)若需要工人进入下水道清理淤泥,打开下水道井盖后首先进行的操作是_________
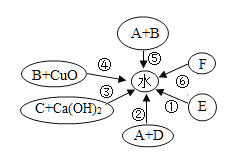
有同学对此类问题进行了定量探究,某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或多种。为确认其组成,某同学取一定量该气体按下图所示装置进行实验(假设每步都充分反应或吸收)
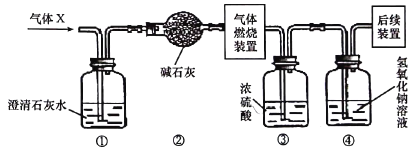
结果装置①中无明显变化,证明气体X成分中一定没有_______,装置③增重1.8g,装置④增重2.2g。则气体X中氢元素的质量为_____,气体X中碳元素的质量为_____。下列关于气体X成分的分析中,错误的是______
A.可能只有甲烷 B.可能含有甲烷和氢气
C.可能含有氢气、一氧化碳和甲烷 D.可能含有氢气和一氧化碳
E.可能含有甲烷和一氧化碳
【题目】实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
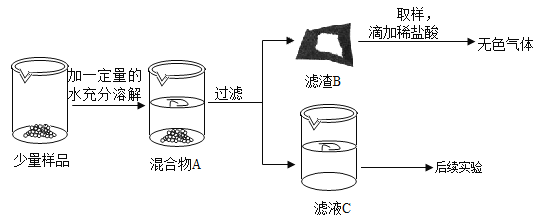
查阅资料:(1)Ca(OH)2、Na2CO3溶于水无明显的温度变化。
(2)CaCl2+Na2CO3=2NaCl+CaCO3↓。
(3)CaCl2溶液呈中性。
(1)滤渣B中一定含有_____,产生该物质的化学方程式可能是___(写出一个即可)。
(2)滤液C成分的探究。
(猜想)滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④____。
(设计方案并进行实验)甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3。
乙同学:取滤液C少许放入试管中,滴加足量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH。
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生。向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3。
(反思与评价)
丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。他认为滤液C中的溶质一定含有________,可能含有NaOH。为进一步确认滤液C中是否含NaOH,请你帮助他设计实验进行验证。
实验操作 | 实验现象 | 实验结论及解释 |
________ | ________ | 猜想④正确 |
(3)实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是__________(填序号)。
① 样品中一定含NaOH ② 样品中一定含Na2CO3
③ 样品中含NaOH、CaO中的一种或两种