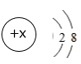题目内容
【题目】如图是元素周期表中的一格及碘原子的结构示意图,下列说法错误的是
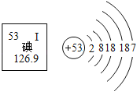
A. 碘原子相对原子质量为126.9,原子核内质子数为53
B. 碘原子核外有53个电子,最外层有7个电子
C. 碘原子最外层电子能量低于倒数第二层电子的能量
D. 碘原子属于非金属元素,碘原子在化学变化中容易得到电子
【答案】C
【解析】
在原子中,核电荷数=核内质子数=核外电子数=原子序数;电子离原子核越远,能量越高;一般情况下,最外层电子数小于4的,在反应中容易失去电子,大于4的,在反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子。
A、根据周期表中的单元格信息,可知碘原子相对原子质量为126.9,原子序数为53,核内质子数=原子序数,故原子核内质子数为53,故A说法正确;
B、碘原子核外有53个电子,最外层有7个电子,故B说法正确;
C、电子离原子核越远,能量越高,故碘原子最外层电子能量高于倒数第二层电子的能量,故C说法错误;
D、碘原子属于非金属元素,碘原子在化学变化中容易得到1个电子形成带1个单位负电荷的碘离子,故D说法正确。故选C。

练习册系列答案
相关题目