题目内容
【题目】实验室从含有 CuSO4、ZnSO4、FeSO4的废液中回收工业原料硫酸锌和有关金属的流程如下: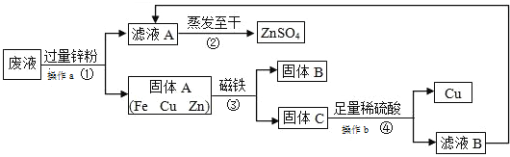
请回答:
(1)操作a、操作b均为__________,该操作用到的玻璃仪器为_____、玻璃棒、烧杯。
(2)滤液 A 和滤液 B 含有相同的溶质,其名称是_____;固体 B 的化学式为_____。
(3)步骤①中加入过量锌粉的目的让废液中的_______完全反应;步骤④加入足量稀硫酸有气泡产生,反应的化学方程式为__________。
(4)该流程中发生的置换反应共有__________个。
【答案】 过滤 漏斗 硫酸锌 Fe CuSO4、FeSO4 Zn+H2SO4=ZnSO4+H2↑ 3
【解析】本题考查了利用金属活动性顺序,回收硫酸锌和有关金属的知识,依据金属活动性顺序及其意义进行分析。
(1)操作a、操作b是将固体和液体的分离,操作a、操作b均为过滤;该操作用到的玻璃仪器为漏斗、玻璃棒、烧杯;
(2)滤液A中的溶质是硫酸铜、硫酸亚铁与锌反应生成的硫酸锌和滤液B是的溶质是锌和硫酸反应产生的硫酸锌,滤液 A 和滤液 B 含有相同的溶质,其名称是硫酸锌;固体B能够被磁铁吸引,因此B是铁;
(3)步骤①加入的过量锌粉与硫酸铜、硫酸亚铁反应,过量锌粉的目的让废液中的CuSO4、FeSO4完全反应;步骤③得到固体C中含有铜和锌,步骤④加入足量稀硫酸与锌反应生成硫酸锌和氢气,其反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑;
(4)流程中发生的置换反应有,锌与硫酸亚铁反应生成硫酸锌与铁,锌与硫酸铜反应生成硫酸锌和铜,硫酸与锌反应生成硫酸锌和氢气,共3个。

【题目】推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。请对下列错误观点举出相应的否定例证(填化学式或化学方程式)。
错误观点 | 否定例证 | |
① | 有单质和化合物生成的反应一定是置换反应 | 举例:CuO+CO |
② | 含氧元素的化合物一定是氧化物 | ___________________ |
③ | 与酸反应放出气体的物质,一定是活泼金属 | _______________ |
④ | 生成盐和水的反应一定是中和反应 | _________________ |
【题目】在进行“二氧化碳制取和性质”的分组实验过程中,某实验小组设计了如图![]() (左a右b)两套制取二氧化碳的装置:
(左a右b)两套制取二氧化碳的装置:
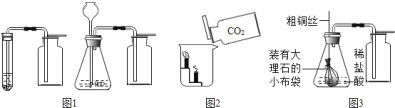
![]() 你认为设计合理的是________(填字母序号),实验室制取二氧化碳的化学反应方程式为:________;
你认为设计合理的是________(填字母序号),实验室制取二氧化碳的化学反应方程式为:________;
![]() 用正确的装置制取一瓶二氧化碳后,乙同学做了如图
用正确的装置制取一瓶二氧化碳后,乙同学做了如图![]() 所示验证二氧化碳性质的实验,请和实验小组的同学一起完成下列实验报告册的填写:
所示验证二氧化碳性质的实验,请和实验小组的同学一起完成下列实验报告册的填写:
实验现象 | _________ |
实验结论 | ________ |
![]() 实验结束后反应还在继续,丙同学觉得浪费了化学药品,于是对上述装置进行了如图
实验结束后反应还在继续,丙同学觉得浪费了化学药品,于是对上述装置进行了如图![]() 所示的改进.请回答:
所示的改进.请回答:
丁同学认真分析后,觉得该装置还可以用来制取氧气,写出用该装置制取氧气的化学反应方程式:________.