题目内容
某物质4.6克在空气中燃烧生成了8.8克二氧化碳和5.4克水,关于该物质的下列说法正确的是( )
| A、该物质中一定含的碳元素、氢元素,可能含有氧元素 |
| B、该物质中一定含有碳元素、氢元素、氧元素 |
| C、该物质中一定含有碳元素,氢元素,一定没有氧元素 |
| D、该物质中碳元素与氢元素的原子个数比为1:2 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律的含义(即六不变)中的“元素的种类不变”可知,生成物所含的碳、氢、氧三种元素中的碳元素和氢元素一定来自于有机物,至于氧元素可能全部来自于氧气,也可能部分来自于氧气,另一部分则来自于4.6g物质,可根据元素的质量不变进行判断;根据生成物CO2和H2O中C、H元素质量,让碳氢元素的质量分别除以各自的相对原子质量再相比,就可以得到该物质中碳氢两元素的原子个数比.
解答:解:由化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数可知:
8.8g二氧化碳中碳元素的质量=8.8g×
×100%=2.4g;
5.4g水中氢元素的质量=5.4g×
×100%=0.6g;
根据质量守恒定律知:生成物中的碳、氢两元素来自该物质,
又由于2.4g+0.6g=3g<4.6g,
说明该物质一定含有碳、氢两元素,而且还一定含有氧元素.所以选项A、C错误,B正确;
该物质中碳、氢元素的原子个数比=
:
=1:3,所以选项D错误.
故选B.
8.8g二氧化碳中碳元素的质量=8.8g×
| 12 |
| 44 |
5.4g水中氢元素的质量=5.4g×
| 2 |
| 18 |
根据质量守恒定律知:生成物中的碳、氢两元素来自该物质,
又由于2.4g+0.6g=3g<4.6g,
说明该物质一定含有碳、氢两元素,而且还一定含有氧元素.所以选项A、C错误,B正确;
该物质中碳、氢元素的原子个数比=
| 2.4g |
| 12 |
| 0.6g |
| 1 |
故选B.
点评:本题主要考查质量守恒定律的应用及相关计算,根据反应前后元素的质量和种类不变,元素质量比=A相对原子质量×A原子个数:B相对原子质量×B原子个数,推导出:原子个数比=
进行解答,要认真分析.
| 元素质量比 |
| 相对原子质量比 |

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
属于缓慢氧化的变化的是( )
| A、木炭燃烧 | B、蜡烛燃烧 |
| C、食物腐败 | D、汽油燃烧 |
下列关于溶液的说法正确的是( )
| A、溶液中溶质的溶解度随温度的升高而增大 |
| B、一定温度下,将 NaCl晶体磨碎,可以增大其在水中的溶解度 |
| C、20℃时,向KNO3溶液中加入少量KNO3晶体,溶质的质量分数一定增大 |
| D、向100g10%的NaCl溶液中加入10gKCl,全部溶解,所得溶液中NaCl的质量分数一定减小 |
关于一氧化碳气体的叙述错误的是( )
| A、有可燃性,可作燃料 |
| B、有还原性,可用于冶炼金属 |
| C、可以与人体的血红蛋白结合 |
| D、是一种有刺激性气味的气体 |
下列选项中都有Ⅰ、Ⅱ、Ⅲ三种溶液,在Na2CO3溶液中加入Ⅰ溶液,产生白色沉淀,再加入Ⅱ溶液,沉淀溶解,并有气泡产生,然后再继续加入Ⅲ溶液,又产生白色沉淀.符合上述变化的Ⅰ、Ⅱ、Ⅲ选项分别是( )
| A、CaCl2 HNO3 KCl |
| B、CaCl2 HNO3 AgNO3 |
| C、BaCl2 H2SO4 CuCl2 |
| D、BaCl2 HCl NaOH |
某元素的原子结构示意图如图,对该元素的有关认识正确的是( )
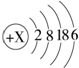

| A、该元素位于元素周期表中的第六周期 |
| B、该元素是金属元素 |
| C、该元素原子的最外层电子数是2 |
| D、该元素的原子核内质子数是34 |
学好化学,就要学会归纳和总结,下列总结有错误的一组是( )
| A、安全常识 沼气爆炸──CH4引起 煤气中毒──CO引起 |
| B、生活知识 硬水──可溶性的钙镁化合物含量高蜂窝煤易于燃烧──与空气充分接触 |
| C、性质与用途 H2作高能燃料──可燃性 CO炼铁──还原性 |
| D、物质分类 空气──混合物 河水──氧化物 |
现有100g一氧化碳和二氧化碳混合气,测得碳的质量分数为24%,将混合气依次通入灼热的氧化铜完全反应后,再通入足量澄清的石灰水后,得到最大沉淀量为( )
| A、100克 | B、150克 |
| C、200克 | D、185克 |
