题目内容
下列选项中都有Ⅰ、Ⅱ、Ⅲ三种溶液,在Na2CO3溶液中加入Ⅰ溶液,产生白色沉淀,再加入Ⅱ溶液,沉淀溶解,并有气泡产生,然后再继续加入Ⅲ溶液,又产生白色沉淀.符合上述变化的Ⅰ、Ⅱ、Ⅲ选项分别是( )
| A、CaCl2 HNO3 KCl |
| B、CaCl2 HNO3 AgNO3 |
| C、BaCl2 H2SO4 CuCl2 |
| D、BaCl2 HCl NaOH |
考点:盐的化学性质
专题:常见的盐 化学肥料
分析:在Na2CO3溶液中加入Ⅰ溶液,产生白色沉淀,说明沉淀是碳酸盐沉淀,加入Ⅱ溶液,沉淀溶解,并有气泡产生,说明加入的是酸,再继续加入Ⅲ溶液,又产生白色沉淀,说明该沉淀不溶于酸.
解答:解:A、CaCl2和HNO3符合题意,但是加入KCl后不能生成不溶于酸的沉淀,故A错;
B、碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,加入硝酸,硝酸能与碳酸钙反应生成硝酸钙、水和二氧化碳;再加入硝酸银,由于溶液中存在氯化钠,所以氯化钠与硝酸银反应生成氯化银白色沉淀,不溶于硝酸,故B正确;
C、碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,加入硫酸,硫酸与碳酸钡反应生成硫酸钡沉淀、水和二氧化碳,由于硫酸钡沉淀不溶于酸,所以沉淀不能溶解,故C错;
D、氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,加入盐酸,盐酸与碳酸钡反应生成氯化钡、水和二氧化碳,再加入氢氧化钠不会生成沉淀,故D错.
故选B.
B、碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,加入硝酸,硝酸能与碳酸钙反应生成硝酸钙、水和二氧化碳;再加入硝酸银,由于溶液中存在氯化钠,所以氯化钠与硝酸银反应生成氯化银白色沉淀,不溶于硝酸,故B正确;
C、碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,加入硫酸,硫酸与碳酸钡反应生成硫酸钡沉淀、水和二氧化碳,由于硫酸钡沉淀不溶于酸,所以沉淀不能溶解,故C错;
D、氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,加入盐酸,盐酸与碳酸钡反应生成氯化钡、水和二氧化碳,再加入氢氧化钠不会生成沉淀,故D错.
故选B.
点评:解答本题关键是要知道,加入酸才能将沉淀溶解,加入酸后,再加入一种试剂出现白色沉淀,说明该白色沉淀不溶于酸.

练习册系列答案
相关题目
手机中使用的是锂离子电池.已知锂离子(Li+)的原子核中质子数为3,中子数为4,下列有关锂离子的说法,正确的是( )
| A、原子核外的电子数为3 |
| B、相对质量比锂原子小得多 |
| C、原子的核电荷数为+1 |
| D、原子核外的电子数为2 |
下列实验操作或记录正确的是( )
| A、稀释浓硫酸时,将水沿烧杯壁慢慢倒入浓硫酸中,并用玻璃棒不断搅拌 |
| B、打开装有浓盐酸的试剂瓶,可看到白烟 |
| C、用托盘天平称取5.4g氯化钠 |
| D、用10mL量筒量取9.54mL水 |
下列实验操作错误的是( )
A、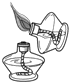 |
B、 |
C、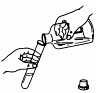 |
D、 |
某物质4.6克在空气中燃烧生成了8.8克二氧化碳和5.4克水,关于该物质的下列说法正确的是( )
| A、该物质中一定含的碳元素、氢元素,可能含有氧元素 |
| B、该物质中一定含有碳元素、氢元素、氧元素 |
| C、该物质中一定含有碳元素,氢元素,一定没有氧元素 |
| D、该物质中碳元素与氢元素的原子个数比为1:2 |
人体健康离不开化学,下列叙述正确的是( )
| A、氧、碳、氢、氮、钠、铁是人体所需的常量元素 |
| B、健康人体内胃液的pH范围是0.5~1.9 |
| C、为预防甲状腺肿大,应在食盐中添加大量的碘元素 |
| D、在人类食物所供给总能量中,有60%~70%来自糖类 |
下列有关书写化学方程式的原则或步骤,叙述错误的是( )
| A、必须遵守质量守恒定律 |
| B、一定要注明反应条件 |
| C、要注明生成物的状态(气体、沉淀) |
| D、在化学方程式配平的过程中,需要改动化学式的下标,这样可使配平容易一些 |