题目内容
【题目】镓(Ga)是灰蓝色或银白色的金属,主要用于电子工业和通讯领域,是制取各种镓化合物半导体的原料。下图是元素周期表中提供的镓元素的部分信息及镓原子的结构示意图。下列有关说法错误的是
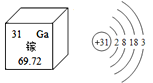
A. 镓元素位于第四周期,其原子核外共有31个电子
B. 镓元素属于非金属元素,镓原子在化学反应中容易得到电子
C. 镓的相对原子质量为69.72,原子核内质子数为31
D. 氧化镓的化学式为Ga2O3,其中镓元素的化合价为+3价
【答案】B
【解析】A.镓元素核外有四个电子层,位于第四周期,原子序数是31,其原子核外共有31个电子,故A正确;B. 镓元素属于金属元素,镓原子在化学反应中容易失去到电子,故B错误;C.镓的相对原子质量为69.72,原子核内质子数为31,故C正确;D.氧化镓的化学式为Ga2O3,氧通常显-2价,根据正负总价代数和为零原则,其中镓元素的化合价为+3价,故D正确。
点睛∶原子序数等于核内质子数等于核外电子数。

 应用题作业本系列答案
应用题作业本系列答案【题目】钙是人体中的常量元素,因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2.请根据有关信息回答问题。
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入盐酸的质量(g) | 20 | 20 | 20 | 20 |
剩余固体的质量(g) | 35 | 30 | a | 20 |
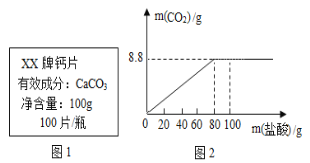
(1)a的数值为_____。
(2)该品牌补钙药剂中CaCO3的质量分数是_____?该盐酸中溶质的质量分数是多少?_____(写出计算过程,计算结果精确至0.1%)
【题目】根据如图回答问题:
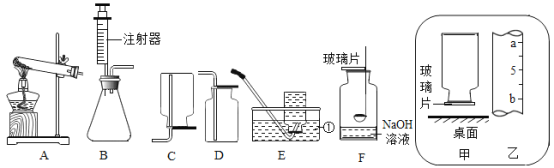
(1)写出图中标号仪器名称:①_____。
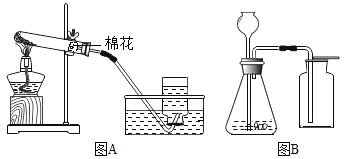
(2)实验室用高锰酸钾制取并收集一瓶比较干燥的氧气,应选用的装置组合为_____(填字母,从装置A--E中选择),还缺少一种实验用品,其作用为_____。写出高锰酸钾制氧气的文字表达式_____。
(3)某兴趣小组在实验室用B装置来制取氧气,反应后要回收二氧化锰固体,应对反应后的混合物进行的实验操作是_____、洗净、干燥。
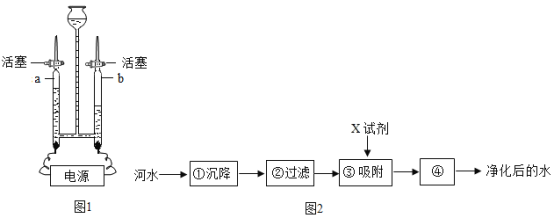
(4)用F装置做硫在氧气中的燃烧实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住瓶口并振荡,若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来(如图甲),则F装置中NaOH溶液的作用是_____。为了完成上述实验,用10mL量筒量取6mL的NaOH溶液,读数时量筒内液体的凹液面最低处应与乙图中_____处(填“a”或“b”)刻度线保持水平。
(5)我们知道氧气能使带火星的木条复燃,那么使带火星的木条复燃是否一定需要纯氧呢?为了弄清这个问题,某化学探究小组进行了如下探究:
Ⅰ.取5个大小相同的集气瓶,分别编号1、2、3、4、5,并分别使瓶内留有占集气瓶10%、20%、30%、40%、50%的水(余下的为空气),用玻璃片盖住,并倒扣于装有水的水槽中。
Ⅱ.分别用排水法向上述5个瓶中通入氧气,小心把5个瓶内的水排完用玻璃片盖住瓶口,取出正立放好。
Ⅲ.分别将带火星的木条伸入5个瓶中,现象如下:
编号 | 1 | 2 | 3 | 4 | 5 |
现象 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
根据实验回答下列问题
①从观察到的现象可知,使带火星的木条复燃所需氧气的最小体积介于_____ 号瓶和_____号瓶之间。
②用排水法收集氧气后,4号瓶中氧气的体积分数约为_____。
【题目】实验室配制50g质量分数为20%的硝酸钾溶液,现有25g溶质质量分数为40%的硝酸钾溶液、20g溶质质量分数为15%的硝酸钾溶液及足量的硝酸钾固体和水,请选用上述药品设计三种配制方案,并填入下表:
配制方案(只要说明配制所需的各种药品及用量即可) | |
方案一 |
|
方案二 |
|
方案三 |
|