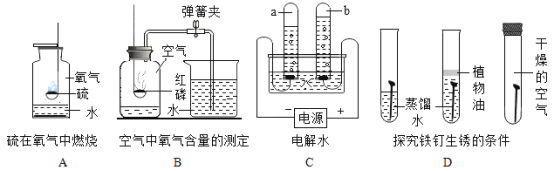
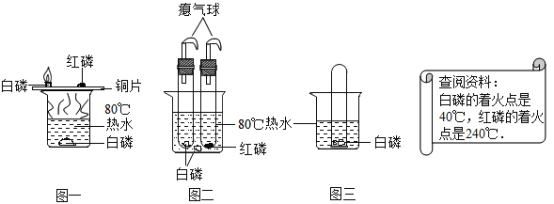
题目内容
【题目】请结合下列实验装置,回答有关问题:
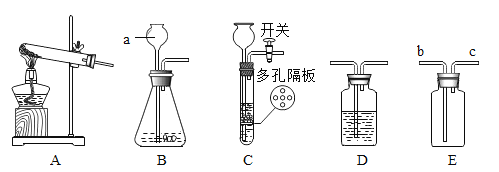
(1)写出标号a仪器的名称______________。
(2)实验室用A装置制取O2的方程式为______________。
(3)实验室制取CO2的方程式为______________,若要获得干燥的二氧化碳,还应选用D装置,并在该装置中盛放______________(填写试剂名称)。如果用E装置收集CO2气体,则气体从_____________端进入(填“b”或“c”)。
(4)硫化氢(H2S)是有毒气体,能溶于水形成氢硫酸(其化学性质与盐酸相似)。常用块状硫化亚铁(FeS)和稀硫酸在常温下发生复分解反应制H2S。
①实验室制取H2S气体的化学方程式为______________。
②制取H2S气体时,可将B装置改进为C装置,其改进后的优点是______________。
(5)工业上以氨气为原料制备硝酸的过程(见图1)如下:
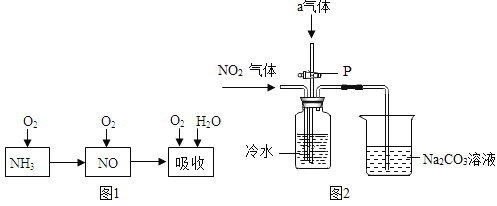
某课外小组认真分析了工业制取硝酸的流程及反应原理,设计了如图2的实验装置制备硝酸,试回答下列相关问题:
①完成图1工业上用氨气制取NO的化学方程式: ![]() ____________。然后产生的NO 被氧气氧化成NO2;在“吸收”步骤中,发生反应的化学方程式为
____________。然后产生的NO 被氧气氧化成NO2;在“吸收”步骤中,发生反应的化学方程式为![]() 。
。
②连接好图2装置后,首先进行的操作是______________。
③图2中通入的气体a是______________;Na2CO3 溶液的作用是______________。
(6)配制30g 10%的 Na2CO3溶液,步骤为:计算、称取、量取、__________、转移。
①如果配制的碳酸钠溶液溶质的质量分数偏小,其原因可能是______________。
A转移称量好的固体时,有固体洒落在桌面上
B量水时俯视读数
C转移配制好的溶液时,有少量液体溅出
D溶解固体的烧杯用水润湿
②若要将30g 10%的 Na2CO3溶液稀释为2%的Na2CO3溶液,需要加水______________g。
【答案】长颈漏斗 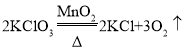
![]() 浓硫酸 b
浓硫酸 b ![]() 可以控制反应的发生和停止 H2O 检查装置的气密性 氧气 吸收未反应的二氧化氮 溶解 AD 120g
可以控制反应的发生和停止 H2O 检查装置的气密性 氧气 吸收未反应的二氧化氮 溶解 AD 120g
【解析】
(1)仪器a为长颈漏斗;
(2)A装置适用于固体加热反应制取氧气,试管口无棉花,可用氯酸钾和二氧化锰加热制取氧气,该反应的化学方程式为: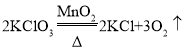 ;
;
(3)实验室常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,该反应的化学方程式为:![]() ;
;
若要获得干燥的二氧化碳,还应选用D装置,浓硫酸具有吸水性,且二氧化碳不与浓硫酸反应,故可在该装置中盛放浓硫酸;
二氧化碳密度大于空气,如果用E装置收集CO2气体,则气体从b端进入;
(4)①常用块状硫化亚铁(FeS)和稀硫酸在常温下发生复分解反应制H2S,复分解反应为“两种化合物互相交换成分,生成另外两种化合物”的反应,故该反应的化学方程式为:![]() ;
;
②制取H2S气体时,可将B装置改进为C装置,其改进后的优点是:可以控制反应的发生和停止,将块状硫化亚铁置于隔板上,关闭止水夹,通过长颈漏斗添加稀硫酸,使固液接触,反应发生生成硫化氢气体,装置内压强增大,将稀硫酸压入长颈漏斗内,固液分离,反应停止,打开止水夹,固液接触,反应发生;
(5)①根据质量守恒定律,化学反应前后,原子的种类和数目不变,故图1工业上用氨气制取NO的化学方程式为:![]() ;
;
②连接好图2装置后,首先进行的操作是检查装置的气密性;
③图2中通入的气体a是氧气,因为![]() ;
;
NO2有毒,未反应的二氧化氮排放到空气中会污染空气,Na2CO3 溶液的作用是:吸收未反应的二氧化氮;
(6)配制30g 10%的 Na2CO3溶液,步骤为:计算、称取、量取、溶解、转移;
①A、转移称量好的固体时,有固体洒落在桌面上,溶质质量变小,故溶质质量分数偏小,符合题意;
B、量水时俯视读数,读取数值大于实际数值,量取的水的体积偏小,溶液质量偏小,溶质质量分数偏大,不符合题意;
C、溶液具有均一、稳定性,转移配制好的溶液时,有少量液体溅出,溶质质量分数不变,不符合题意;
D、溶解固体的烧杯用水润湿,溶剂的质量偏大,溶液的质量偏大,溶质质量分数偏小,符合题意。
故选AD。
②若要将30g 10%的 Na2CO3溶液稀释为2%的Na2CO3溶液,设需要加水的质量为x,30g×10%=(30g+x)×2%,x=120g。