题目内容
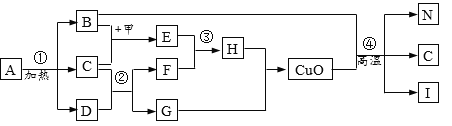
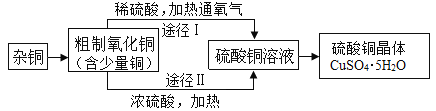
【题目】硫酸铜的制备如图为某兴趣小组用含较多杂质的铜粉制取硫酸铜晶体[CuSO45H2O]的两种实验方案。
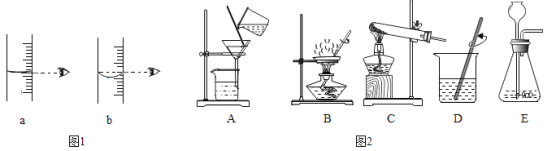
(1)制备中需过滤得到硫酸铜晶体。过滤时需要的玻璃仪器有烧杯、玻璃棒和______。
(2)灼烧杂铜除去其中的杂质,产生CO2和少量CO.灼烧后的产物为CuO及少量Cu.产物中含有Cu的可能原因是______(填序号)。
A灼烧过程中,部分氧化铜与一氧化碳反应
B灼烧不充分,铜未被完全氧化
C该条件下铜无法被氧气氧化
(3)方案Ⅰ通入氧气,少量Cu转化为CuSO4.该反应的化学方程式为______。
(4)方案Ⅱ中加入浓硫酸发生的反应有Cu+2H2SO4=CuSO4+SO2↑+2H2O
方案Ⅰ优于方案Ⅱ的理由是______。
【答案】漏斗 AB 2Cu+O2+2H2SO4![]() 2CuSO4+2H2O 不会产生污染大气的气体
2CuSO4+2H2O 不会产生污染大气的气体
【解析】
(1)过滤时需要的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)铜在加热条件下易生成氧化铜,氧化铜稳定,难以分解,在灼烧过程中部分氧化铜被还原或者灼烧不充分铜未被完全氧化均会导致杂铜经灼烧后得到的产物含有少量铜,故答案为:AB;
(3)方案Ⅰ通入氧气,少量Cu转化为CuSO4,即铜在氧气和稀硫酸作用下反应生成硫酸铜和水,该反应的化学方程式为2Cu+O2+2H2SO4=2CuSO4+2H2O;
(4)方案Ⅱ中加入浓硫酸发生的反应有Cu+2H2SO4![]() CuSO4+SO2↑+2H2O,方案Ⅰ优于方案Ⅱ的理由是不会产生污染大气的气体;
CuSO4+SO2↑+2H2O,方案Ⅰ优于方案Ⅱ的理由是不会产生污染大气的气体;
故填:
(1)漏斗;
(2)AB;
(3)2Cu+O2+2H2SO4![]() 2CuSO4+2H2O;
2CuSO4+2H2O;
(4)不会产生污染大气的气体。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】取10g锌粉和铜粉的混合物于烧杯中,向烧杯中分四次加入等质量的同种稀硫酸,实验过程中得到如下数据。
第1次 | 第2次 | 第3次 | 第4次 | |
加入稀硫酸的质量 | 20g | 20g | 20g | 20g |
剩余固体的质量 | 8.7g | 7.4g | 6.1g | 5.5g |
(1)混合物中铜粉的质量是________。
(2)所用稀硫酸中溶质的质量分数是_____。(保留计算过程)