题目内容
【题目】实验室配置质量分数为10%的NaCl溶液。如图是某同学的实验操作过程:
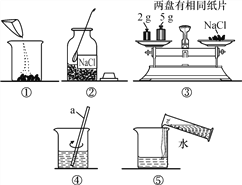
(1)用图中的序号表示配置溶液的正确操作顺序是________,a的名称是________。
(2)若③中游码读数为1.2,则他称取NaCl的质量是________g。
(3)按③中所称NaCl质量来算,该同学需要用水的体积是________mL。(水的密度为1.0 g/mL)
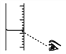
(4)他按如图所示量取水的体积,若其他操作步骤均无误差,则其所配溶液溶质质量分数________(填“大于”“等于”或“小于”)10%。
【答案】 ②③①⑤④ 玻璃棒 5.8 52.2 小于
【解析】(1)配制溶液的基本步骤是计算、称量、量取、溶解,故步骤为②③①⑤④;其中a仪器的名称是玻璃棒;
(2)图中的物体和砝码放反了,故该称量方法中,砝码的质量等于物体的质量加上游码的质量,故物体的质量为:7g-1.2g=5.8g;
(3)5.8g氯化钠可配得10%的氯化钠溶液的质量为: 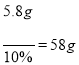 ,故水的质量为:58g-5.8g=52.2g,水的密度为1.0 g/mL,故水的体积为52.2 mL;
,故水的质量为:58g-5.8g=52.2g,水的密度为1.0 g/mL,故水的体积为52.2 mL;
(4)当用量筒量取水的体积仰视读数时,量取的水的实际体积偏大,故所配溶液溶质质量分数小于10%;

 名校课堂系列答案
名校课堂系列答案【题目】某实验小组开展了如下有关碱的化学性质探究活动:

(1)实验1的目的是________________________________________________________________________;
(2)实验2中发生反应的化学方程式是________________________;
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl以外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是________________________;
(4)通过上述实验探究活动,可以总结出碱的化学性质是
①碱能与酸发生中和反应;
②________________;
……
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,该两瓶溶液的溶质质量分数分别为5%和10%。请设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)。
实验步骤 | 预计现象及 相应结论 |
__________________________ | ________________________________为5%的氢氧化钠溶液,另一种为10%的氢氧化钠溶液 |